1. Introducción - Historia
El Nutricionista Clínico (NC) del siglo XXI ha incorporado junto a sus actividades clínicas, un liderazgo destacado en investigación, ya que ejecuta con rigor metodológico y con equipos multidisciplinarios la realización de estudios en los cuales participa desde su formulación, ejecución y hasta su divulgación.
El primer ensayo controlado documentado data de 600 a.C., cuando Daniel de Judea sometió a jóvenes babilonios a una dieta vegetal y comparó sus resultados con los del régimen real (Daniel 1:816). Desde entonces, la nutrición ha evolucionado de simples observaciones a rigurosos estudios multicéntricos:
- 1747- James Lind: a bordo del HMS Salisbury, comparó seis protocolos dietéticos contra el escorbuto y demostró que cítricos frescos (vitamina C) restauraban la salud de los marineros en pocos días, sentando las bases del ensayo clínico moderno.
- 1897 - Christiaan Eijkman: en Java comprobó que el beriberi remitía al sustituir arroz refinado por arroz integral, descubriendo lo que luego se identificó como tiamina (vitamina B₁) y el concepto de nutrientes “esenciales”.
- 1912 - Casimir Funk y Frederick G. Hopkins: acuñaron el término vitamina y postularon la existencia de “factores alimentarios accesorios” cuya carencia ocasiona enfermedad, abriendo la era de la nutrición molecular.
- 1913-1922 - Elmer V. McCollum et al: caracterizaron las vitaminas liposolubles A y D y demostraron su papel en la visión y la mineralización ósea.
- 1941- Food and Nutrition Board (NRC, EE. UU.): publicó las primeras Recommended Dietary Allowances (RDA), integrando datos de balance metabólico y marcando el inicio de la planificación dietética basada en requerimientos cuantificados.
- 1958-1970 - Ancel Keys, Seven Countries Study: analizó >12 000 varones y demostró la asociación entre patrones dietéticos, grasas saturadas y riesgo cardiovascular, legitimando la “dieta mediterránea” como modelo preventivo.
Estos hitos anticiparon la evidencia actual, que demuestra que la intervención nutricional reduce complicaciones, acorta estancias y disminuye costes, aunque aún esté infrautilizada en muchos hospitales (1). Según ESPEN: «A pesar de la alta prevalencia de desnutrición, su gestión no es rutinaria y existen pocas políticas al respecto» (2). Por tanto, la nutrición no es solo un deber ético, sino una estrategia clínica y económica de gran impacto.
Realizar una visión actualizada del desempeño profesional del Nutricionista Clínico dentro de una perspectiva integral que abarca, liderazgo, investigación y aplicación basada en evidencia y la aplicación de herramientas tecnológicas para fortalecer el diagnóstico preciso sobre la base de principios ético que prioricen y protejan al paciente.
El NC enfrenta hoy el reto de participar y liderar la producción de evidencia científica, involucrándose no solo en la aplicación de guías, sino también en su diseño y validación. La formación continua, la inserción en la academia, el trabajo en redes, el dominio de bioética, la economía de la salud y la comunicación científica son pilares del perfil investigador. Se ha resaltado el papel, a menudo subestimado, del nutricionista en la investigación y la importancia de su participación para optimizar resultados clínicos. También se abordan las fortalezas y debilidades de los metaanálisis, así como la necesidad de considerar el costo de las intervenciones para optimizar recursos en salud. Se reconoce la necesidad de sistemas organizados de revisión y actualización en el área bibliográfica y de investigación. A lo largo de esta revisión se ha mostrado cómo los avances científicos han transformado la disciplina, así como los retos que enfrenta el proceso investigativo.
En el recorrido del capítulo se pretende demostrar una visión actualizada del NC donde destaca el desempeño profesional dentro de una perspectiva integral que abarca, liderazgo, investigación aplicación basada en evidencia, con utilización de herramientas tecnológicas- IA -big data- entre otras, para fortalecer el diagnóstico preciso sobre la base de principios ético que garanticen transparencia que prioricen y protejan al paciente. En cuanto a la metodología: para la elaboración de este artículo, se utilizó un enfoque combinado de búsqueda de información. En primer lugar, se empleó una herramienta de inteligencia artificial (un asistente virtual) para realizar un primer rastreo de referencias bibliográficas relevantes en el ámbito de la nutrición y la investigación nutricional. Posteriormente, las referencias sugeridas fueron corroboradas y ampliadas mediante consultas directas en bases de datos académicas, como Google Scholar, Scopus, Web of Science, PubMed identificando así estudios adicionales y literatura científica complementaria.
De esta manera, la metodología combinó el uso de herramientas de búsqueda asistida por IA con la verificación manual y la expansión del marco bibliográfico de forma tradicional, asegurando así un respaldo riguroso y actualizado para los contenidos presentados.
El impulso del investigador
Investigar (lat. investigāre, de vestigium) significa “seguir pistas”: profundizar, analizar y descubrir (2). En ciencia, es buscar lo aún no identificado, pues lo que falta suele ser la clave del avance (2).
La investigación aplicada -casos detallados, técnicas innovadoras y traslación a la práctica- es esencial para la calidad y actualización en salud (3). Ya en 1925, Ladd propuso que los nutricionistas hospitalarios dedicaran la mitad de su jornada a la investigación y a la aplicación práctica de la terapia médiconutricional, considerando esta actividad esencial para el progreso de la disciplina (4). Otros autores compartieron esa visión y reclamaron la participación de los profesionales en estudios clínicos (5).
Décadas más tarde, MacEachan reafirmó la idea: el avance de la nutrición como ciencia -y su traducción a la práctica mediante la dieta - dependía en gran medida de los estudios desarrollados en el entorno clínico (6). Sin embargo, los datos indicaban lo contrario: Noland y Steinberg informaron en 1965 que los nutricionistas dedicaban apenas el 0,6 % de su tiempo laboral a la investigación (7). El informe The Skeleton in the Hospital Closet (1974) reveló el impacto de la desnutrición no diagnosticada en morbilidad y mortalidad (8,9), lo que impulsó equipos multidisciplinarios y nuevos estándares (10-12). Hoy, en la era de la Medicina Basada en la Evidencia (MBE), el nutricionista debe integrarse plenamente en la investigación (12), asumiendo roles de: Asistencia avanzada al paciente hospitalizado, educación nutricional al equipo, generación activa de conocimiento (13,14), con especial énfasis en estudios de nutrición enteral y parenteral en pacientes hospitalizados con diversas patologías.
Expectativas versus realidad
Encuestas en equipos de soporte nutricional muestran una brecha entre deseo y práctica. Schiller halló que el 63 % de los nutricionistas nunca había participado en investigación, pese a que el 70 % expresaba interés (15). Un sondeo de la American Dietetic Association (ADA, 1981) reveló que solo el 15 % de sus miembros dedicaba parte de su tiempo a investigaciones, y la mayoría menos de diez horas semanales (15). Mientras el 90 % de los directores de enfermería y el 80 % de los jefes médicos esperaban esa participación, apenas el 60 % de los administradores reconocía formalmente ese rol.
La American Society for Parenteral and Enteral Nutrition (ASPEN) defiende la paridad de oportunidades investigadoras, pero en sus congresos de 1985-1986 solo el 6,9 % de los trabajos presentados incluían nutricionistas como autores.
Diversos organismos han subrayado la investigación como eje de la profesión(16-19). El plan estratégico de la ADA insiste en que sus miembros sean reconocidos como especialistas en alimentación y salud (20,21). Más recientemente, Howard (Australia, 2013) demostró que la capacidad investigadora de los dietistas se desarrolla gradualmente con la experiencia (22).
Barreras identificadas y consumo de tiempo
El Comité Europeo de Expertos en Nutrición, Alimentación y Salud del Consumidor (1999) señaló los principales obstáculos para una nutrición hospitalaria adecuada (23), y estudios posteriores añadieron otras barreras que consumen tiempo del nutricionista clínico (24): Sobrecarga de trabajo: 25 nutricionistas (34 %), escasa coordinación con enfermería y especialistas: 20 (27 %), responsabilidades interdisciplinarias poco claras: 17 (23 %), recursos limitados en las unidades de soporte: 15 (21 %), gestión hospitalaria deficiente: 11 (15 %), evaluación nutricional exhaustiva y laboriosa: 10 (14 %), problemas de comunicación y formación insuficiente: 10 (14 %), estancias hospitalarias demasiado breves: 10 (14 %), reestructuraciones organizativas frecuentes: 6 (8 %) y falta de retroalimentación sobre el screening nutricional: 5 (7 %).
Screening nutricional: prevención secundaria imprescindible
El cribado (screening) identifica a individuos asintomáticos en riesgo mediante pruebas sistemáticas (23-25). La Organización Mundial de la Salud lo amplía como “la aplicación sistemática de una prueba para identificar sujetos con riesgo suficientemente elevado de un problema de salud, a fin de proponerles una investigación más profunda o una acción preventiva, dentro de una población que no ha buscado atención por síntomas” (25). Su aplicación, liderada por nutricionistas clínicos, es esencial para reducir morbilidad y mortalidad prematuras. Este concepto de screening o cribado se sigue estudiando a profundidad y ampliando su utilización.
Alcance y limitaciones
Se aborda únicamente la investigación aplicada de impacto clínico directo; no se trata en detalle la investigación básica ni la nutrición animal, salvo su relevancia clínica. Los datos epidemiológicos están actualizados a 2025; se recomienda verificar nuevas guías publicadas tras el cierre editorial.
2. Investigación aplicada: del descubrimiento a la práctica clínica
2.1. Investigación en salud: qué es y para qué sirve (26).
La investigación en salud, definida por la Comisión de Investigación en Salud para el Desarrollo como “la generación de nuevos conocimientos mediante el método científico para identificar y controlar problemas de salud” (27), persigue no sólo ampliar nuestra comprensión de la enfermedad y el bienestar, sino también ofrecer soluciones concretas. Aunque a menudo se asocia con el desarrollo de tecnologías y fármacos en países avanzados, gran parte de su valor reside en adaptar y contextualizar estas innovaciones en entornos distintos, garantizando que las intervenciones -desde nuevas pruebas de cribado/ screening hasta herramientas diagnósticas- resulten eficaces en poblaciones específicas (26,28).
2.2. Fases de la investigación aplicada (T0-T4) (29)
La trayectoria desde el laboratorio hasta el paciente se estructura en cinco etapas. En T0 se formulan hipótesis y se generan patentes; T1 verifica la seguridad en humanos; T2 confirma eficacia en ensayos controlados; T3 traduce resultados a protocolos clínicos; y T4 evalúa el impacto poblacional y coste-efectividad mediante cohortes y análisis de big-data (29) (Tabla 1).
Tabla 1:
Fases de la Investigación Aplicada (29)

2.3. Modelos de transferencia de tecnología y conocimiento
La transferencia de conocimiento (TC) es el mecanismo por el cual los hallazgos de laboratorio (T0–T1) se convierten en prácticas clínicas consolidadas (T3–T4). En Nutrición Clínica, todo proceso de TC debe cumplir tres condiciones esenciales:1) Generar valor clínico o económico, demostrando que la innovación mejora la atención o reduce costes. 2) Respetar la integridad ética, garantizando la protección de datos y el bienestar de los pacientes. 3) Retroalimentar al investigador, de manera que las lecciones del despliegue clínico orienten nuevas preguntas y mejoras.
A continuación, se describen los principales modelos de TC, ejemplificando su aplicación y las métricas clave que suelen emplearse para evaluar su éxito:
2.3.1 Modelos de transferencia
- Licenciamiento y spin-offs (nueva narrativa creada de una existente): Una universidad o centro de investigación patenta un descubrimiento y luego lo licencia a una empresa o crea una división propia. Por ejemplo, NutriGenDx© desarrolla un kit de PCR-on-a-chip para detectar intolerancia a lípidos MCT, licenciado a una start-up que alcanzó TRL 9 en tres hospitales. Métricas: ingresos por royalties, número de pacientes tratados y grado de madurez tecnológica (TRL).
- Alianzas público-privadas (PPP): Contratos de cofinanciación que comparten riesgos y beneficios. El convenio NIH–Abbott (2024) para una fórmula enteral sostenible con proteína de lenteja fermentada combina fondos y know-how institucional. Métricas: proporción público/privado de la financiación, tiempo hasta la aprobación sanitaria y número de sitios de ensayo.
- Consorcios de datos abiertos y ciencia colaborativa: Acuerdos FAIR (justos y equilibrados) que permiten compartir grandes volúmenes de historias clínicas anonimizada. La iniciativa GLIM 2.0 mantiene un repositorio OMOP (Observational Medical Data Model Outcomes Partnership) con más de un millón de registros, soportando validaciones diagnósticas y metaanálisis vivientes. Métricas: descargas de datos, citas académicas y aplicaciones clínicas basadas en el dataset.
- Plataformas digitales y APIs (SaMD): Desarrollo de software médico interoperable (FHIR). Nutri-RiskAI es un algoritmo integrado en 15 EHR (electronic health record) de UCI (terapias intensivas) latinoamericanas, con >80 % de adopción por turno. Métricas: sensibilidad/especificidad, tasa de uso y reducción de complicaciones.
- Innovación frugal y social: Prototipos de bajo coste cocreación con usuarios finales. Un ejemplo son las bombas de infusión enteral impresas en 3D para hospitales rurales, validas ISO 10993. Métricas: coste por unidad, tasa de adopción local y sostenibilidad a largo plazo.
- Comunidades de práctica y tele-mentoría: Redes como NutriECHO-ICU organizan sesiones virtuales para intercambiar protocolos y casos clínicos. Métricas: número de sesiones/anual, mejora de la auto-eficacia profesional y datos de resultados clínicos (LOS-tiempo de estancia hospitalaria-, complicaciones).
2.3.2 Herramientas para gestionar la transferencia
Para guiar y monitorizar la Transferencia de Conocimiento en Nutrición Clínica, se emplean:
- TRL (Technology Readiness Levels): escala de 1 a 9 que mide la madurez de la innovación.
- CFIR y RE-AIM: marcos que identifican barreras/ facilitadores (CFIR) y cuantifican alcance, eficacia y mantenimiento (RE-AIM).
- Toolkits de propiedad intelectual: plantillas tipo Lambert o Creative Commons que aceleran acuerdos.
- Dashboards de oficina de transferencia: paneles de control que siguen métricas de patentes, acuerdos firmados, ingresos y adopción clínica.
- Guías de evaluación de tecnologías sanitarias (HTA): procedimientos estandarizados para evaluar coste-efectividad, impacto organizativo y ético antes de la escalada.
2.3.3. Buenas prácticas y criterios de éxito
Una transferencia exitosa descansa sobre cuatro pilares interdependientes:
- Estrategia temprana de propiedad intelectual-patente, secreto industrial u open-source- definida antes de divulgar resultados. 2. Evaluación económica rigurosa (health-technology assessment) que acompaña los ensayos T2 para demostrar costo-efectividad y facilitar la adopción. 3. Gobernanza ética sólida que incorpore la voz de los pacientes y se alinee con Declaraciones Internacionales de la Federación Latinoamericana de Nutrición Enteral y Parenteral (FELANPE), Sociedad Europea de Nutrición Enteral y Parenteral (ESPEN), así como de los Códigos y 4. Plan de sostenibilidad ambiental que cuantifique la huella de carbono (ISO 14067) y priorice el diseño circular.
2.4. Estrategias para acortar la brecha de implementación
Reducir de dos décadas a menos de siete años el tiempo que transcurre entre el descubrimiento y la aplicación clínica requiere, en paralelo: 1. La conformación temprana de equipos verdaderamente multidisciplinarios - nutriólogos, estadísticos, ingenieros y bioeticistas - que diseñan los estudios con una visión T0-T4; 2. La consolidación de redes interoperables de datos clínicos basadas en estándares FHIR (Fast Healthcare Interoperability Resources), que define recursos normalizados y métodos REST (operaciones básicas en arquitecturas web para consultar y modificar datos), y en el modelo de datos común OMOP, que unifica y estructura registros electrónicos para estudios observacionales, resulta esencial para validar biomarcadores y entrenar algoritmos de inteligencia artificial a gran escala. 3. La integración de IA responsable en las historias electrónicas, auditada para minimizar sesgos y capaz de anticipar y prevenir la malnutrición; y 4. El despliegue de ensayos adaptativos y descentralizados, más ágiles y costo-efectivos, que facilitan la inclusión de poblaciones tradicionalmente sub-representadas.
2.5. Niveles de desarrollo de la investigación clínica
La American Dietetic Association identifica cuatro niveles progresivos en los que el nutricionista puede implicarse en actividades investigativas, desde la aplicación inmediata de conocimientos hasta la dirección estratégica de proyectos multicéntricos (15, 30,31).
Nivel 1: Práctica. En esta fase inicial, el profesional utiliza de forma crítica la literatura científica y herramientas metodológicas básicas para resolver problemas cotidianos en la atención nutricional. Se centra en incorporar hallazgos ya validados (por ejemplo, guías de hidratación o protocolos de soporte nutricional) de manera reflexiva, revisando constantemente las fuentes y aplicándolas directamente al cuidado del paciente. El dominio de búsquedas bibliográficas, lectura crítica y síntesis de evidencia constituye la habilidad esencial en este nivel.
Nivel 2: Colaboración. Al avanzar, el nutricionista comienza a traducir la experiencia asistencial en publicaciones internas, informes de caso y contribuciones a guías clínicas de su institución. Participa activamente en equipos multidisciplinares, aporta datos y ayuda a redactar manuscritos o presentaciones. Aquí se establece el puente entre la práctica diaria y el mundo académico: la experiencia del “campo” se convierte en material de estudio y referencia para colegas, favoreciendo la estandarización de procesos y el desarrollo de recomendaciones basadas en la realidad local.
Nivel 3: Participación. En este estadio, el profesional adquiere responsabilidades en el diseño y ejecución de estudios originales: elabora el protocolo, coordina la recolección de datos y colabora en el análisis estadístico. Su rol evoluciona de colaborador a co-investigador, asumiendo tareas como la gestión de cuestionarios, la supervisión de ensayos piloto o la revisión de la validez de los instrumentos de medición. El objetivo es generar nuevos conocimientos y contribuir a la literatura internacional mediante ensayos clínicos, cohortes o registros específicos.
Nivel 4: Liderazgo. Finalmente, el nutricionista alcanza la capacidad de concebir y dirigir líneas de investigación propias. Aquí asume la iniciativa en la obtención de fondos competitivos, la creación de consorcios y la coordinación de proyectos multicéntricos. Desarrolla políticas institucionales de investigación, diseña estrategias de transferencia de tecnología y supervisa equipos de trabajo. Su rol estratégico implica no solo generación de evidencia, sino también la definición de agendas científicas y la influencia en la toma de decisiones sanitarias a nivel regional o nacional.
Cada transición entre niveles se construye sobre la experiencia y las competencias adquiridas previamente: la aplicación reflexiva de la evidencia (nivel 1) inspira colaboraciones (nivel 2), que a su vez forman la base para la realización de estudios originales (nivel 3) y, finalmente, para el desarrollo de liderazgo investigador (nivel 4)(15,30,31).
2.6. Procesos iniciales para implementar investigación en salud
Todo proyecto clínico sigue seis pasos interdependientes. Primero, se define la pregunta de investigación, vinculándola a necesidades reales del entorno asistencial. A continuación, se realiza una revisión sistemática de la literatura para detectar vacíos y evitar duplicaciones. Con esa base, se elige el diseño metodológico más adecuado (observacional, experimental o mixto) y se elabora el protocolo, que luego debe aprobar un comité de ética para asegurar la protección de los participantes. Tras su visto bueno, se recogen los datos con instrumentos validados y se analizan mediante estadística apropiada. Finalmente, los resultados se interpretan críticamente y se difunden para impulsar mejoras en la práctica clínica.
Empezar con estudios de bajo coste- por ejemplo, series de casos o encuestas validadas- acelera la curva de aprendizaje, fortalece la colaboración interinstitucional y allana el camino para ensayos multicéntricos más complejos. Actualmente, en algunos países, organismos como el Ministerio de Agricultura y otros sectores destinan fondos y recursos competitivos para la investigación (32).
2.7. El nutricionista investigador: liderazgo, competencias y compromiso con la investigación
Para que el nutricionista evolucione de simple consumidor de evidencia a generador activo de conocimiento, es esencial incorporar la investigación como hilo conductor de su formación- desde la carrera de grado hasta el posgrado- y ofrecer espacios de capacitación avanzada que incluyan módulos metodológicos rigurosos, estancias en centros de investigación y redes interinstitucionales de intercambio de datos. Este enfoque fomenta no solo la curiosidad científica, sino también el desarrollo de competencias transversales en gestión de proyectos, comunicación científica, bioética y economía de la salud, indispensables para garantizar la calidad, la sostenibilidad y la pertinencia de los estudios (33).
El liderazgo investigador se manifiesta en la participación estratégica en comités académicos y clínicos, la coordinación de equipos multidisciplinarios, la obtención y gestión de fondos competitivos, y la mentoría de nuevas generaciones. Al posicionar al nutricionista como agente activo en la definición de agendas científicas, se potencia su visibilidad ante colegas, financiadores y la sociedad, consolidándolo como referente en innovación terapéutica y mejora continua de la atención sanitaria.
A pesar de estas oportunidades, encuestas como las de la Dietetics Practice-Based Research Network identifican barreras significativas: la falta de tiempo protegido, las limitaciones de recursos institucionales, la escasa formación específica en investigación y la percepción de que ésta es una función secundaria frente a las tareas clínicas (34). No obstante, la Academy of Nutrition and Dietetics resalta que los dietistas-nutricionistas registrados deben integrar de forma permanente la investigación en su práctica, colaborar en los grandes desafíos de la nutrición, expandir su impacto a nivel de sistemas de salud y contribuir a la erradicación de la malnutrición a escala global (34).
En conjunto, el compromiso activo con la investigación- respaldado por una formación sólida, el desarrollo de competencias clave y el apoyo instituciona- permite al nutricionista clínico no solo aplicar la evidencia existente, sino también generar nuevos hallazgos que impulsen la excelencia y la innovación en el cuidado nutricional.
2.8. Diseño, ámbitos y requisitos de la investigación en nutrición clínica
La investigación en nutrición clínica debe sustentarse en principios metodológicos rigurosos que aseguren su validez y aplicabilidad. Desde la formulación de la pregunta hasta la difusión de resultados, cada estudio debe planificarse con objetivos claros, empleando métodos objetivos y verificables, cuantificando efectos y estableciendo relaciones causales que contemplen el componente sociocultural del conocimiento. Abrir la puerta a hipótesis alternativas y valorar siempre la utilidad práctica de los hallazgos garantiza que los nuevos conocimientos no queden relegados al ámbito académico, sino que se integren de manera efectiva en la atención diaria de los pacientes.
Este marco metodológico se despliega en diversos campos de aplicación. La investigación biomédica básica explora mecanismos fisiológicos y metabólicos, tanto en entornos hospitalarios como ambulatorios; los estudios en servicios de alimentación optimizan procesos para entregar dietas seguras y adaptadas; la investigación clínica evalúa cómo las intervenciones nutricionales modifican la evolución de enfermedades; y los análisis de coste-beneficio justifican la asignación de recursos, demostrando la eficiencia económica de las terapias nutricionales en hospitales y en atención ambulatoria.
Para impulsar y sostener esta agenda científica, resulta indispensable contar con una base formativa sólida y un entorno institucional comprometido. La tutoría académica - a través de tesis de máster y doctorado- y los programas de formación avanzada dotan al nutricionista de herramientas metodológicas y experiencia práctica. La inclusión del profesional en equipos de investigación hospitalarios, gubernamentales y de ONGs favorece la colaboración interdisciplinaria y el acceso a datos reales. Al mismo tiempo, es imprescindible disponer de infraestructura adecuada, libre de conflictos de interés, que permita desarrollar proyectos relevantes y reproducibles.
Finalmente, debe existir un entorno que valore y recompense la actividad investigadora. Mejorar la remuneración y los incentivos a la publicación no solo motiva a los nutricionistas a dedicar tiempo y esfuerzo a la investigación, sino que también garantiza la sostenibilidad de las líneas de trabajo. Solo así, combinando rigurosidad metodológica, campos de aplicación bien definidos y un apoyo institucional y económico firme, podrá la investigación en nutrición clínica transformar el cuidado nutricional y generar valor tangible en la salud de las personas
2.8.1. Pasos operativos para un proyecto de investigación en nutrición clínica (35).
La investigación se entiende aquí como una indagación rigurosa, crítica y sistemática orientada a generar o ampliar conocimiento útil para la práctica clínica. En nutrición, esa búsqueda puede implicar un hallazgo disruptivo o la validación de una idea previa; lo esencial es seguir un itinerario metodológico transparente y reproducible.
- Formulación de la pregunta y revisión bibliográfica: Toda investigación parte de una pregunta clara: ¿qué se estudia, ¿quién lo hará, ¿cómo, dónde y ¿cuándo? Antes de diseñar el estudio, es imprescindible revisar exhaustivamente la literatura existente para ubicar el proyecto en el contexto adecuado, identificar vacíos de conocimiento y refinar objetivos que sean específicos y alcanzables. Esta fase evita duplicaciones y orienta la selección del diseño más apropiado, ya sea prospectivo, aleatorio o mixto, con criterios de calidad bien definidos.
- Selección del diseño y población diana: La naturaleza de la pregunta dicta el enfoque metodológico: estudios observacionales (transversales, retrospectivos o de cohorte) resultan útiles para explorar asociaciones en pacientes reales, mientras que los ensayos clínicos intervencionistas- incluidos diseños adaptativos o n-de-1- aportan evidencia de causalidad. Asimismo, el metaanálisis es un “ensayo sobre papel” que sintetiza múltiples RCT homogéneos. En esta fase se define con precisión la población de interés, así como criterios de inclusión y exclusión, para asegurar la validez interna y externa del estudio (Tabla 2).
Tabla 2:
Principales características y aplicaciones de diferentes tipos de estudios epidemiológicos de nutrición (36).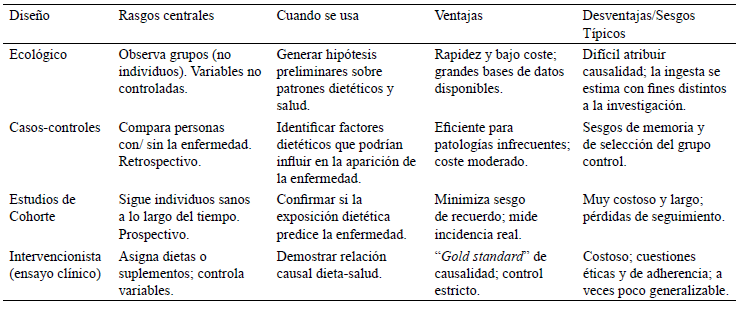
- Elaboración del protocolo y aprobación ética: Con el diseño definido, se redacta el protocolo detallando variables independientes (causas) y dependientes (resultados clínicos), el cálculo del tamaño muestral y los procedimientos de control de sesgos. Es esencial contar con asesoría estadística desde la fase inicial y someter el documento a un comité de ética, junto al plan de consentimiento informado. Este filtro garantiza la seguridad de los participantes y la transparencia del estudio.
- Recolección de datos y análisis estadístico: Durante la fase de campo, se emplean fichas estandarizadas y controles de calidad - verificación en tiempo real, respaldo de datos y registro de versiones- para minimizar errores. Es fundamental anticipar las principales fallas en la recolección de datos, como muestras demasiado pequeñas que reducen el poder estadístico o el sesgo de no participación derivado de altas tasas de rechazo de los sujetos de estudio (39). El análisis combina estadística descriptiva (medias, desviaciones, frecuencias) con pruebas inferenciales (t-Student, ANOVA, regresión o modelos mixtos) que permitan evaluar la significancia y la magnitud del efecto. Los resultados han de interpretarse con cautela, reconociendo limitaciones y proponiendo estudios de seguimiento si persisten incertidumbres.
- Financiación sostenible: El investigador elabora un resumen ejecutivo breve que justifique la relevancia, el diseño y el presupuesto (laboratorio, personal, logística, análisis y difusión). A partir de allí, explora fuentes de financiación: oficinas de I+D universitarias, agencias nacionales, fundaciones, ministerios y consorcios públicoprivados. La transparencia en el uso de recursos y la anticipación de costes fortalecen la credibilidad y facilitan la gestión de futuros proyectos.
- Publicación y difusión del conocimiento: Tras el análisis final, el manuscrito sigue el formato IMRyD (Introducción, Métodos, Resultados y Discusión) adaptado al alcance de la revista destino. Debe incluir carta al editor, declaraciones de financiación y conflictos de interés, registro en plataformas como ClinicalTrials.gov o PROSPERO, y enlaces a repositorios de datos abiertos (OSF, GitHub). Además, pósteres, presentaciones orales, infografías y presencia en redes sociales amplían el impacto clínico y científico, transformando la publicación en punto de partida para nuevas investigaciones y colaboraciones.
3. Medicina y Nutrición Basadas en Evidencia
La práctica clínica moderna ya no se sustenta en la intuición o la tradición, sino que exige conocer con precisión por qué y con qué solidez se opta por una intervención u otra. En este contexto surge la Medicina Basada en Evidencia (MBE) y su vertiente nutricional, la Nutrición Basada en Evidencia (NUBE), que proporcionan un marco metodológico para transformar datos en decisiones fundamentadas, reproducibles y transparentes. El término “evidencia” ha ganado protagonismo en la literatura clínica, epidemiológica y en los documentos de salud pública y políticas sanitarias, reflejando un auténtico giro epistemológico: la experiencia profesional debe contrastarse de manera sistemática con hallazgos de investigación de alta calidad y con los valores y preferencias de cada paciente (16). Así, la MBE se define como «la utilización consciente, explícita y juiciosa de la mejor evidencia disponible para tomar decisiones sobre la atención de pacientes individuales» (37).
Una decisión clínica plenamente fundamentada descansa en la convergencia de tres dominios complementarios. En primer lugar, se apoya en la mejor evidencia disponible, que abarca desde estudios básicos en biomedicina hasta ensayos clínicos y series centradas en el paciente, evaluando la exactitud diagnóstica, el poder predictivo de los marcadores y la eficacia y seguridad de las intervenciones; esta evidencia se revisa y actualiza continuamente, permitiendo reemplazar prácticas obsoletas por opciones más precisas y seguras. En segundo lugar, integra la experiencia clínica, es decir, la pericia acumulada del profesional para identificar rápidamente el estado de salud y los riesgos de cada persona y calibrar el balance beneficio–riesgo de las distintas alternativas. Finalmente, incorpora los valores y preferencias del paciente, que incluyen creencias, expectativas y condicionantes socioculturales o económicos; reconocerlos y respetarlos no solo favorece la adherencia terapéutica, sino que humaniza la atención. Sólo al armonizar evidencia científica, juicio clínico y valores personales se establece una auténtica alianza diagnóstica y terapéutica que optimiza los resultados y la calidad de vida de los pacientes (37).
3.1. Niveles de clasificación y calidad de la información
En la toma de decisiones clínicas, no todas las fuentes de información tienen igual peso: en la cúspide de la pirámide de evidencia se sitúan los ensayos clínicos aleatorizados de alta calidad y las revisiones sistemáticas homogéneas, seguidos de los estudios de cohortes, casos-controles y series de casos; en la base, la opinión de expertos. Guyatt et al. estructuran este gradiente en niveles que van desde el 1A (la evidencia más sólida) hasta el 2C (evidencia observacional con alto riesgo de sesgos) (38). Si bien un ensayo controlado y aleatorizado bien diseñado supera la suma de múltiples series de casos, incluso los metaanálisis pueden verse comprometidos por la heterogeneidad entre estudios o el sesgo de publicación, lo que subraya la necesidad de una lectura crítica que valore la metodología, la consistencia de los resultados y la aplicabilidad al contexto local.
Aunque existen diversas escalas de clasificación - que pueden variar según el país, la especialidad o el autor- lo esencial es reconocer que los ensayos clínicos controlados al azar representan la evidencia más confiable cuando cumplen los criterios básicos de aleatorización, control de factores de confusión y minimización de sesgos. A continuación, se presenta la jerarquía propuesta por Guyatt et al. en User’s Guides to the Medical Literature (39) (Tabla 3).
Tabla 3:
Niveles de evidencia (39)

Aún existen criterios de selección que tienen en cuenta variables como costos y riesgos de sesgos, los cuales pueden ser útiles al elegir la duración del estudio epidemiológico (36) (Tabla 4).
Tabla 4:
Principales errores en los métodos de recolección de datos en estudios epidemiológicos de nutrición (39)
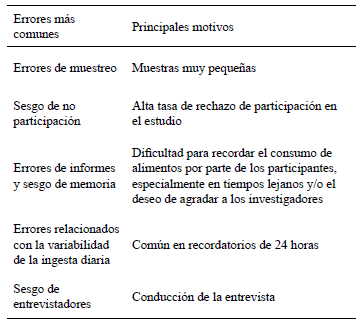
Los errores en la recolección de datos sobre el consumo de alimentos pueden evitarse mediante la recolección repetida de datos, la aplicación de diferentes métodos y el uso de marcadores biológicos de exposición.
Después de la recolección de datos, los nutrientes consumidos estimados dependen de los datos disponibles en tablas validadas por diferentes investigadores (36).
3.3. Medicina basada en evidencias, un nuevo “paradigma”
Desde su consolidación en los años noventa, la Medicina Basada en Evidencia (MBE) ha supuesto un auténtico cambio de paradigma en la atención sanitaria (40). Tal como describió Sackett en el *British Medical Journal*, la MBE “es el uso consciente, explícito y criterioso de la mejor evidencia disponible para tomar decisiones sobre el cuidado de pacientes individuales” (40).
El mérito de la MBE radica en su metodología precisa y en la jerarquización de la información: los ensayos clínicos controlados aleatorizados y los metaanálisis de calidad encabezan la pirámide de evidencia, seguidos por estudios de cohorte, casos-controles y series de casos, mientras que la opinión de expertos ocupa la base. Gracias a este orden, las intervenciones con impacto poblacional- aún moderado para cada individuo- solo se visibilizan cuando se cuantifican en grandes muestras, permitiendo estandarizar tratamientos de enfermedades comunes que antes variaban según costumbres o escuelas de pensamiento (41-43). Además, la MBE protege a la comunidad frente a terapias no validadas o impulsadas por intereses comerciales, concentrando el gasto en procedimientos comprobados (41).
Este enfoque se opone a la medicina autoritaria o al simple razonamiento fisiopatológico sin respaldo experimental, y adopta la noción de paradigma de Kuhn para subrayar que hoy es impensable una práctica clínica que no remita a evidencias rigurosas (44). Hoy, la MBE trasciende el ámbito estrictamente médico e impregna disciplinas como la salud pública (SPBE), la odontología (OBE), la fisioterapia (FBE), la nutrición clínica (NUBE) y la medicina veterinaria (MVBE) (45). Su expansión se alimenta de tres motores: en primer lugar, el acceso ilimitado a la información - bibliotecas electrónicas en abierto, repositorios indexados- que democratiza el conocimiento y acelera la actualización de protocolos; en segundo lugar, la incorporación de la lectura crítica y la estadística aplicada en los planes de estudio de ciencias de la salud, de modo que los egresados dominen los cinco pasos de la MBE antes de iniciar su práctica (46); y, por último, la aparición de metodologías innovadoras - ensayos adaptativos, plataformas pragmáticas y evidencia del mundo real - que generan datos más rápidos y generalizables al aprovechar registros electrónicos, biosensores y big data.
De cara al futuro inmediato, surgen tendencias que ya modelan la práctica clínica: la inteligencia artificial rastrea y sintetiza literatura en tiempo real, creando recomendaciones personalizadas; los ensayos adaptativos ajustan su diseño según resultados interinos para optimizar recursos y proteger a los participantes; y la evidencia proveniente del mundo real, extraída de historias clínicas electrónicas y apps de seguimiento dietético, valida las intervenciones en poblaciones vulnerables de forma más representativa.
Para el nutricionista clínico, dominar la MBE/ NUBE es hoy una competencia nuclear. En primer lugar, racionaliza la avalancha informativa al filtrar estudios de calidad, identificar lagunas y priorizar lecturas esenciales. En segundo lugar, sostiene decisiones transparentes ante comités éticos, pagadores o auditorías, demostrando el coste efectividad y la seguridad de las intervenciones. Y, finalmente, mantiene el foco en la persona, integrando evidencia, pericia profesional y valores del paciente para elaborar planes de alimentación realmente personalizados. Quien no incorpore estos principios corre el riesgo de quedar desfasado en un entorno que demanda juicio crítico, solvencia estadística y actualización permanente, ahora también apoyada en la inteligencia artificial y los macrodatos.
3.4. Nutrición Basada en Evidencia: origen, particularidades y metaanálisis
La Nutrición Basada en Evidencia (NUBE) surge como adaptación imprescindible de la Medicina Basada en Evidencia (MBE), aplicando sus principios al área nutricional para establecer recomendaciones clínicas y comunitarias sólidas (44,46). Este paradigma nace de la constatación de cuatro carencias: la escasa presencia de la nutrición en muchas revisiones MBE centradas en fármacos; el riesgo de que paneles sin especialistas en nutrición sobrevaloren datos sin considerar la pericia clínica o los valores del paciente; el énfasis terapéutico que omite la prevención y la educación; y la necesidad de profesionales capaces de liderar guías específicas (1).
Pese a la sólida base metodológica heredada de la MBE - con jerarquías que sitúan a los ensayos aleatorizados y a las revisiones sistemáticas en la cúspide -, la investigación en nutrición enfrenta limitaciones éticas y logísticas. A menudo resulta inviable formar grupos sin intervención o aislar el efecto exclusivo de un nutriente en la evolución clínica (47). Los nutrientes, al interactuar con tratamientos farmacológicos y factores metabólicos, genéticos y ambientales, presentan efectos modulados y más débiles, lo que dificulta demostrar evidencias de nivel A en contextos rutinarios. Adicionalmente, la extrapolación de asociaciones poblacionales a nivel individual puede incurrir en falacias ecológicas, y la imposibilidad de aleatorizar estados nutricionales graves plantea dilemas éticos insalvables en ciertos ensayos (47).
Para el nutricionista clínico, estas restricciones exigen diseñar ensayos en los que la variable de resultado tenga significado real (reducción de complicaciones no fatales, prolongación de la vida o mejoras en parámetros funcionales) y complementar, cuando haga falta, con estudios observacionales de calidad o consensos de expertos transparentes (41). Reconocer la interdisciplinariedad de la investigación - que conecta Nutrición Clínica con Nutrición Comunitaria y Básica - permite aprovechar enfoques mixtos y enriquecer el conocimiento global.
En este contexto, las revisiones sistemáticas y los metaanálisis adquieren un papel central: al combinar resultados de múltiples estudios, aumentan el poder estadístico y equilibran el sesgo de pequeños ensayos individuales (42, 43, 48). Sin embargo, su eficacia depende de la calidad de los trabajos incluidos, de la homogeneidad metodológica y de la representatividad de las poblaciones estudiadas. Un metaanálisis cuyo efecto protector supere el 40 % tiene solo un 60 % de probabilidad de replicarse en un ensayo mayor posterior (48), lo que obliga al clínico a evaluar críticamente la consistencia de los métodos dietéticos y la aplicabilidad de sus conclusiones a su propia práctica.
En definitiva, la NUBE consolida un enfoque que, pese a sus desafíos, combina la rigurosidad de la MBE con una adaptación cuidadosa a las particularidades de la nutrición, utilizando metaanálisis para sintetizar evidencia cuando sea posible y recurriendo a metodologías flexibles y consensos cuando la generación de datos de nivel A resulte impracticable.
3.5. De la teoría a la consulta: aplicar la MBE en Nutrición Clínica
La Medicina Basada en Evidencia (MBE) aplicada a la nutrición clínica (NUBE) estructura un itinerario sistemático que convierte la ciencia en decisiones centradas en el paciente. Lejos de ser un ejercicio intuitivo, este enfoque potencia la experiencia profesional y orienta la investigación local hacia vacíos detectados en la revisión crítica de la literatura. Cada vez que surge una duda clínica, el nutricionista formula una pregunta relevante - por ejemplo, en prevención, diagnóstico, pronóstico o tratamiento - y realiza una búsqueda sistemática de la mejor evidencia disponible, priorizando ensayos aleatorizados, revisiones sistemáticas y metaanálisis. A continuación, evalúa la validez interna, la magnitud del efecto y la aplicabilidad al contexto específico del paciente y del sistema de salud. Integrada con su experiencia y los valores y preferencias del paciente, la evidencia guía una intervención personalizada que, finalmente, se audita para medir su eficacia y eficiencia y retroalimentar mejoras continuas (38).
Según la naturaleza del problema, el profesional puede adoptar distintos “modos” de práctica: el modo actualización, para cuestiones frecuentes que requieren búsqueda y lectura crítica constantes; el modo evaluación, cuando es preciso reexaminar prácticas consolidadas a la luz de nueva evidencia; y el modo innovación, al abordar preguntas sin respuesta clara que pueden motivar investigaciones propias o colaborativas. La aplicación rigurosa de estos pasos alcanza tres objetivos: estandarizar intervenciones y reducir la variabilidad individual, fundamentar decisiones ante comités y financiadores mostrando su relación coste-efectividad, y mejorar resultados clínicos estableciendo una alianza diagnóstica-terapéutica basada en evidencia, pericia y valores del paciente (38).
Para ilustrar este proceso, consideremos el manejo nutricional en sepsis: la pregunta “¿qué estrategia de alimentación enteral reduce más la estancia hospitalaria?” conduce a consultar bases de datos y guías (ESPEN, ASPEN, FELANPE), valorar la tolerancia gastrointestinal, los recursos disponibles y el contexto sociocultural, y adaptar las recomendaciones a las necesidades individuales. Toda decisión queda documentada en la historia clínica, citando la evidencia y justificando los ajustes realizados.
Sin embargo, la experiencia clínica, aunque insustituible, puede introducir sesgos y automatismos si no se complementa con evidencia formal40. Herramientas validadas como GLIM, NRS-2002 o MUST, MNA -SF, fortalecen este abordaje, mejorando diagnósticos, intervenciones coste efectivas y el monitoreo de la respuesta terapéutica. Aun así, la MBE enfrenta críticas: algunos cuestionan la calidad y neutralidad de la evidencia - a menudo generada o financiada por la industria - y su reduccionismo biomédico que podría marginar factores emocionales, culturales y éticos (41). Reconocer estas limitaciones no implica rechazar la MBE, sino enriquecerla con un juicio clínico crítico y contextualizado, manteniendo siempre el foco en la persona.
En definitiva, la MBE/NUBE ofrece al nutricionista clínico una brújula metodológica que filtra la sobrecarga informativa, sustenta decisiones con transparencia y refuerza la calidad y seguridad de la atención. Su implementación rigurosa no solo da respuesta a los retos actuales, sino que impulsa la mejora continua del cuidado nutricional y la generación de nueva evidencia que nutra el ciclo de la práctica clínica.
3.6. Revisiones sistemáticas y metaanálisis: fortaleza y límites
Las revisiones sistemáticas - y, cuando procede, los metaanálisis - ocupan la cúspide de la pirámide de evidencia al agrupar resultados de múltiples estudios, depurar heterogeneidad e incrementar la precisión de las estimaciones de efecto (42,43). Su principal virtud es reducir la variabilidad terapéutica y ofrecer un marco sólido para el desarrollo de guías clínicas y la evaluación de tecnologías sanitarias, al basarse en datos reproducibles que mitigan la influencia de sesgos comerciales y facilitan decisiones transparentes.
No obstante, su potencia estadística no las exime de limitaciones. El sesgo de publicación, la disparidad metodológica entre los ensayos incluidos y la escasa representatividad de contextos locales pueden distorsionar las conclusiones (43). En nutrición clínica, estas limitaciones se acentúan debido a la escasez de grandes ensayos por razones éticas y logísticas, y al exceso de literatura que puede saturar al profesional si no emplea filtros críticos eficaces. Por ello, el nutricionista debe ir más allá del resumen: evaluar la calidad de las búsquedas, la consistencia de los datos y la aplicabilidad de los hallazgos a su población antes de extrapolar recomendaciones.
En definitiva, las revisiones sistemáticas y los metaanálisis refinan -pero no reemplazan- el arte clínico: señalan dónde la ciencia aporta certezas y dónde la prudencia, la experiencia y la compasión de los profesionales deben prevalecer, recordándonos que la mejor evidencia siempre requiere una interpretación ética y contextualizada (41).
3.7. Argumento económico: coste-beneficio de la intervención nutricional (49,50).
La desnutrición hospitalaria afecta a más del 10 % -infradiagnosticada- de los pacientes y su tratamiento tardío aumenta las complicaciones y prolonga las estancias hasta un 70 - 300 % más de coste (51). Bajo el lema “Avanzar la nutrición del paciente”, ASPEN propone seis acciones clave -cultura institucional, diagnóstico precoz, intervención rápida, monitorización, comunicación y continuidad tras el alta- para optimizar resultados y reducir gastos (50). La Nutrición Basada en Evidencia (NUBE) cumple así una doble función: mejorar la eficacia clínica y demostrar la rentabilidad de las intervenciones, protegiendo los presupuestos sanitarios.
Estudios multicéntricos han cuantificado este ahorro. Stratton et al. (2003) estimaron un sobrecoste de 766 € por paciente en riesgo de desnutrición (52), confirmando hallazgos similares en 2007(53) y en la revisión de Ulibarri (2007) (54). Datos más recientes señalan incrementos de costos hospitalarios entre 30 % en Colombia (38) y hasta 54 % en adultos sépticos en EE. UU (55); reingresos y mortalidad también aumentan en pacientes desnutridos (56).
En Brasil (57) la intervención precoz ahorra US $ 92,24 por día evitado y hasta US $ 3 698,92 por muerte prevenida (57), mientras que en EE. UU. la desnutrición podría costar hasta 150 000 M USD al año en complicaciones y reingresos (58).
Modelos de coste-efectividad recientes en España demuestran que cada euro invertido en la “Alliance to Advance Patient Nutrition” se recupera en 3,4 meses, generando ahorro neto desde el segundo trimestre (50). Esto refuerza la máxima clínica: “alimentar bien cuesta menos que tratar las consecuencias de no hacerlo.”
Además del coste directo, existen “costos ocultos” asociados al deterioro físico, mayor morbilidad, recuperación más lenta, uso excesivo de recursos y prolongación de la hospitalización. El Instituto Americano de Medicina (IOM) recomienda evaluar el coste-beneficio de la atención incluyendo seguridad del paciente, aplicación de la MBE y enfoque centrado en valores y necesidades (59).
3.7.1. Evidencia clínica de la rentabilidad nutricional
La intervención nutricional temprana reduce complicaciones moderadas y mejora la ingesta energética y proteica, con ganancia de peso e IMC (60). Su coste-efectividad en pacientes quirúrgicos ancianos ha sido destacada por Oliveira (2009) (61), mientras que Gómez Candela (2010) (62) demostró reducciones en mortalidad y estancia en geriatría y oncología. Errores en el soporte-terapia- nutricional generan costes estimados en 17-29.000M USD anuales en EEUU (63) y las re-hospitalizaciones imprevistas suman millones más (64).
Metaanálisis y ensayos aleatorizados recientes ofrecen la evidencia más sólida: la suplementación guiada por dietistas, iniciada precozmente, reduce la mortalidad (OR 0,65–0,79), disminuye readmisiones no electivas y mejora ingesta y peso (57,65); el estudio EFFORT y la síntesis de Gomes et al. confirman estos beneficios (57,58,65). No obstante, la adición de micronutrientes no siempre mejora la mortalidad más allá de la nutrición estándar (66), y en el perioperatorio el impacto sobre la mortalidad es menos claro (67).
3.7.2. Rentabilidad y posicionamiento profesional
Cuantificar los costes y los resultados clínicos - integrando indicadores económicos en la investigación- fortalece el papel del nutricionista dentro del sistema sanitario. La nutrición adecuada reduce los gastos hospitalarios al prevenir complicaciones y acortar estancias; la rápida prescripción de nutrientes y el trabajo coordinado del equipo de apoyo son fundamentales para maximizar la eficiencia y la calidad de la atención (52, 68).
4. Inteligencia Artificial: una aliada en la generación de evidencia en nutrición.
La Inteligencia Artificial (IA) se ha convertido en una herramienta transformadora para la nutrición, automatizando procesos y aportando modelos predictivos que optimizan tanto la atención clínica como la investigación. Gracias al aprendizaje automático y la minería de datos, los nutricionistas pueden identificar patrones complejos de respuesta a dietas, anticipar riesgos nutricionales y elaborar recomendaciones más precisas, lo que se traduce en intervenciones más oportunas y efectivas.
La capacidad de procesar grandes volúmenes de información (big data) permite analizar hábitos dietéticos y perfiles metabólicos a escala masiva, generando hipótesis de forma ágil y con un nivel de detalle inalcanzable con metodologías tradicionales. Así, algoritmos predictivos estiman el riesgo de desnutrición o complicaciones metabólicas, mientras que la minería de historias clínicas extrae correlaciones que pasarían inadvertidas en un análisis manual.
En esta era centrada en los datos, el nutricionista debe integrar la IA como aliado estratégico: no solo como un soporte tecnológico, sino como una extensión de su pericia clínica, capaz de afinar diagnósticos y personalizar planes alimentarios a la medida de cada paciente.
4.1. Aplicaciones Relevantes de la Inteligencia Artificial en Nutrición y rol del profesional
La Inteligencia Artificial (IA) transforma la nutrición clínica al ofrecer herramientas que automatizan el análisis de datos y potencian la personalización de los planes alimentarios. Entre sus aplicaciones más relevantes se cuentan la minería de historias clínicas, los algoritmos predictivos, los asistentes virtuales y el análisis de ingesta mediante imágenes.
Mediante minería de historias clínicas, los sistemas de IA procesan grandes volúmenes de registros médicos para identificar correlaciones entre dietas previas, respuestas fisiológicas y desenlaces clínicos. Esto permite a los nutricionistas diseñar recomendaciones ajustadas a condiciones específicas - por ejemplo, optimizar protocolos para pacientes con diabetes tipo 2 o enfermedad cardiovascular- basándose en la evidencia acumulada.
Los algoritmos predictivos emplean modelos estadísticos avanzados para anticipar riesgos nutricionales como la malnutrición- desnutrición-, respuesta inflamatoria o la sarcopenia en diferentes poblaciones con énfasis en la población geriátrica. Al identificar señales tempranas, el profesional puede intervenir antes de que aparezcan síntomas clínicos, mejorando significativamente los resultados y la calidad de vida de sus pacientes.
Los asistentes virtuales, integrados en aplicaciones móviles o plataformas web, ofrecen recordatorios de comidas, seguimiento del progreso y retroalimentación instantánea sobre la ingesta. Esto favorece la adherencia al plan nutricional y permite ajustar calorías o micronutrientes en tiempo real, aportando apoyo continuo entre consultas.
La visión por computadora aplicada al análisis de imágenes de platos facilita la estimación automática de porciones y macronutrientes con un simple clic en la cámara del teléfono. Este enfoque supera las imprecisiones de los diarios alimentarios tradicionales y reduce el sesgo de registro, agilizando la monitorización y el ajuste de intervenciones.
Para aprovechar al máximo estas innovaciones, el nutricionista debe asumir un nuevo rol colaborativo y multidisciplinario. En primer lugar, requiere formación continua en IA, minería de datos y estadística para comprender los principios de los algoritmos y evaluar con criterio la validez de sus salidas. Asimismo, debe adaptarse a herramientas digitales, familiarizándose con software especializado, plataformas de seguimiento y aplicaciones de análisis automatizado.
La creación e implementación de soluciones de IA exige colaboración estrecha con ingenieros y desarrolladores. Juntos pueden diseñar algoritmos predictivos personalizados, construir interfaces intuitivas y validar los sistemas en entornos reales. El nutricionista aporta el conocimiento clínico necesario para definir variables relevantes, mientras los ingenieros aseguran que las herramientas sean robustas y escalables.
4.2. Criterios Éticos y Calidad de Datos
La aplicación de la IA en nutrición exige un estricto marco ético y un control riguroso de la calidad de los datos. En primer lugar, la privacidad y la protección de datos son innegociables: los nutricionistas deben garantizar el tratamiento confidencial de la información de los pacientes, cumpliendo con normativas como el GDPR (Reglamento general de protección de datos) y sus equivalentes locales. Asimismo, la transparencia es esencial; los usuarios han de comprender cómo y para qué se emplean sus datos, quién accede a ellos y de qué manera influyen en su atención.
La calidad de los datos determina la fiabilidad de los algoritmos: registros completos, precisos y libres de errores reducen el riesgo de conclusiones inexactas que puedan dañar al paciente. Por ello, antes de entrenar modelos, es responsabilidad del equipo nutricional validar las fuentes y depurar cualquier inconsistencia. El consentimiento informado complementa este proceso, asegurando que el paciente otorgue su permiso tras entender claramente el uso que se dará a su información.
Finalmente, es crucial abordar el sesgo (bias) en los datos y en los propios algoritmos. Cuando los conjuntos de entrenamiento no reflejan la diversidad de la población, las recomendaciones pueden resultar injustas o ineficaces para ciertos grupos. Los nutricionistas, en colaboración con ingenieros, deben identificar y corregir estos sesgos para que las soluciones de IA sean equitativas y verdaderamente beneficiosas para todos los pacientes.
4.3. Métodos Estadísticos Contemporáneos y Big Data en Nutrición
La integración de big data y métodos estadísticos avanzados ha abierto nuevas oportunidades en el campo de la nutrición. Estos enfoques permiten manejar y analizar grandes volúmenes de datos, lo que mejora la toma de decisiones, la predicción de riesgos y la personalización de tratamientos. A través de estas tecnologías, los nutricionistas ahora pueden tener acceso a información mucho más detallada y precisa, lo que permite crear planes nutricionales más específicos y efectivos para cada paciente.
4.3.1. Ómicas y Nutrición de Precisión (69- 71)
Las ómicas son un conjunto de tecnologías de alto rendimiento que permiten estudiar los componentes biológicos de los seres vivos de una manera integral. En el ámbito de la nutrición, se destacan principalmente la genómica, metabolómica y proteómica, cada una con un enfoque distinto pero complementario. Estas tecnologías están permitiendo avanzar hacia una nutrición más personalizada, basada en las características únicas de cada individuo.
- Genómica: Se refiere al estudio del genoma, es decir, el conjunto completo de genes en un organismo. La genómica permite identificar variantes genéticas que pueden influir en la forma en que un individuo metaboliza los nutrientes, responde a dietas específicas o es susceptible a enfermedades relacionadas con la nutrición. Por ejemplo, algunos individuos pueden tener una predisposición genética para metabolizar grasas de manera más eficiente que otros, lo que puede influir en su capacidad para seguir una dieta baja en grasas.
- Metabolómica: Se enfoca en el estudio de los metabolitos, es decir, las pequeñas moléculas producidas durante los procesos metabólicos del cuerpo. La metabolómica puede proporcionar información crucial sobre el estado metabólico de un paciente y cómo sus procesos bioquímicos responden a diferentes nutrientes. Esta información puede ser utilizada para ajustar dietas y suplementos nutricionales de manera mucho más precisa, adaptadas a las necesidades metabólicas del paciente.
- Proteómica: El estudio de las proteínas, o proteómica, examina el conjunto completo de proteínas producidas por un organismo. Las proteínas son esenciales para las funciones celulares y, a menudo, son indicadores importantes del estado nutricional y de salud. A través de la proteómica, se pueden identificar biomarcadores específicos que indican deficiencias nutricionales o enfermedades metabólicas.
Nutrición de precisión es el enfoque que integra estos avances ómicos para personalizar el tratamiento nutricional en función de las características genéticas, metabólicas y proteómicas de cada individuo (69). Gracias a estos avances ómicos, es posible adaptar recomendaciones dietéticas a subgrupos específicos o a cada paciente, optimizando la eficacia clínica y potenciando la prevención de enfermedades. Este enfoque supera los protocolos universales al ajustar la composición y la dosificación de nutrientes según el perfil biológico único de cada persona, mejorando los resultados y reduciendo el riesgo de respuestas adversas (71-72).
4.3.2. Aplicación de la IA sobre Big Data
La Inteligencia Artificial potencia estos métodos al ofrecer algoritmos capaces de extraer patrones complejos de grandes bases de datos nutricionales y clínicos. Los modelos predictivos anticipan el riesgo de malnutrición, sarcopenia o enfermedades metabólicas antes de que aparezcan síntomas, lo que facilita intervenciones tempranas. Un ejemplo reciente es MUST Plus, una herramienta de machine learning validada en un estudio multicéntrico (73) que, integrada en la historia clínica electrónica, detecta riesgo de malnutrición en pacientes hospitalizados con alta sensibilidad y especificidad. Su éxito depende de contar con suficiente personal dietista y formación adecuada, pero demuestra que cualquier sistema de salud puede entrenar modelos propios a partir de sus datos para mejorar el cribado y acelerar la atención nutricional.
El procesamiento de lenguaje natural automatiza el cribado, analizando notas médicas para localizar deficiencias o poblaciones vulnerables con mayor rapidez y precisión. Asimismo, el análisis masivo de patrones dietéticos procedentes de encuestas electrónicas o registros poblacionales permite identificar tendencias y guiar recomendaciones a gran escala. En las UCI ya se emplean redes neuronales entrenadas con datos de miles de pacientes para calcular requerimientos calóricos individualizados y optimizar la recuperación. Estos avances, unidos a la evidencia acumulada en revisiones sistemáticas sobre la validez de los algoritmos de cribado, consolidan a la IA como pieza clave en la prevención y manejo temprano de la malnutrición y otras complicaciones nutricionales.
4.3.3. Ventajas del enfoque multidimensional
La sinergia entre Big Data, técnicas estadístico matemáticas, ómicas e IA ofrece un enfoque verdaderamente multidimensional: fusiona datos genéticos, metabólicos y de comportamiento con registros clínicos y epidemiológicos, enriqueciendo el diagnóstico y la prescripción nutricional. Esto no solo potencia la identificación de nuevas correlaciones y la generación de hipótesis innovadoras, sino que también acelera la traslación de la investigación a la práctica, reduciendo la variabilidad de la atención y mejorando la eficiencia en el uso de recursos.
Al incorporar estas tecnologías, los nutricionistas pueden anticipar riesgos, personalizar planes con precisión milimétrica y monitorizar en tiempo real, elevando la calidad y la seguridad de los cuidados nutricionales.
4.4. Innovaciones Emergentes: Ensayos Descentralizados y Monitorización Remota
La digitalización de los ensayos clínicos y la monitorización remota están redefiniendo la investigación nutricional y la práctica clínica, al permitir seguir a los participantes sin necesidad de visitas presenciales. Este enfoque resulta especialmente valioso en enfermedades crónicas, condiciones complejas y poblaciones con movilidad reducida, pues aumenta la adherencia al estudio y facilita la personalización de las intervenciones.
El reclutamiento virtual se ha convertido en un pilar de los ensayos descentralizados: mediante plataformas digitales, los nutricionistas pueden inscribir y dar seguimiento a pacientes de cualquier ubicación geográfica, eliminando barreras logísticas y ampliando la inclusión de grupos tradicionalmente subrepresentados (áreas rurales, movilidad limitada, horarios restringidos). Esto no solo democratiza el acceso a la investigación, sino que enriquece los datos al incorporar mayor diversidad de perfiles y hábitos alimentarios.
La monitorización remota aprovecha wearables dispositivos electrónicos portátiles que registran en tiempo real parámetros como ritmo cardíaco, actividad física y sueño) y kits de recolección domiciliaria para obtener datos continuos. Los wearables se integran con aplicaciones móviles que suministran al nutricionista información sobre gasto energético y respuestas metabólicas. De igual modo, los kits domésticos - para análisis de sangre, microbiota o composición corporal- permiten un seguimiento constante de biomarcadores (glucosa, vitaminas, minerales), reduciendo visitas clínicas y ofreciendo datos precisos para ajustar dietas y suplementos sin interrumpir la rutina del paciente.
Al combinar estas innovaciones, los ensayos descentralizados y la monitorización remota no solo mejoran la eficiencia y el alcance de la investigación en nutrición, sino que elevan la calidad de la atención individualizada, asegurando intervenciones más oportunas y basadas en datos reales obtenidos en el entorno cotidiano del paciente.
5. Consideraciones Éticas y de Equidad en la Nutrición
La práctica de la nutrición, al igual que otros campos de la salud, está intrínsecamente relacionada con cuestiones éticas y de equidad. A medida que avanzan las tecnologías y las metodologías científicas, los nutricionistas se enfrentan a nuevos dilemas éticos y responsabilidades que deben manejar con rigor y profesionalismo. Este apartado aborda los aspectos fundamentales relacionados con la ética, la equidad, y las implicaciones bioéticas en la nutrición, así como las responsabilidades profesionales que los nutricionistas deben considerar en su ejercicio diario.
5.1. Nutrición en Poblaciones Vulnerables y con Inequidades
La nutrición es un derecho humano fundamental, pero el acceso a una nutrición adecuada no siempre es igual para todos. Las poblaciones vulnerables, como los niños, personas de la tercera edad, comunidades rurales y de bajos recursos, enfrentan barreras significativas que afectan su acceso a alimentos saludables y a terapias nutricionales adecuadas. Estas inequidades, tanto en el acceso como en la calidad de la atención nutricional, requieren que los nutricionistas sean particularmente conscientes de las disparidades sociales, económicas y culturales que afectan a estos grupos.
El nutricionista clínico tiene la responsabilidad ética de identificar y abordar estas desigualdades. Además de proporcionar atención individualizada, el nutricionista debe abogar por políticas públicas que garanticen la equidad en la atención nutricional. Esto incluye la promoción de la justicia distributiva, asegurando que los recursos nutricionales y los beneficios de la atención sean distribuidos de manera equitativa, especialmente hacia los grupos más desfavorecidos.
5.2. Transparencia, Conflicto de Intereses y «Open Science»
La transparencia es un principio ético esencial en cualquier investigación o práctica profesional, especialmente en nutrición. Los nutricionistas, como profesionales de la salud, deben manejar los datos de manera clara y abierta, permitiendo que los pacientes comprendan completamente los procesos que afectan su bienestar. En este contexto, el conflicto de intereses es un tema clave, ya que puede influir en la objetividad del nutricionista y comprometer la calidad de los cuidados proporcionados.
La tendencia hacia la “ciencia abierta” o “open science” promueve la transparencia en la investigación científica, el acceso libre a los datos y la publicación de resultados sin restricciones. Esto contribuye a mejorar la calidad de la nutrición clínica, permitiendo que todos los profesionales accedan a los mismos conocimientos y prácticas basadas en la evidencia.
Los nutricionistas deben adherirse a principios éticos en su investigación, como la declaración de conflictos de interés y la transparencia algorítmica cuando utilizan herramientas de IA. Esto asegura que tanto la ciencia como la práctica nutricional se basen en principios de integridad y responsabilidad.
5.3. Consideraciones Bioéticas en la Investigación Nutricional
La bioética es un campo fundamental en la investigación nutricional, que asegura que las prácticas y los estudios se realicen respetando los derechos humanos y los principios éticos. En la investigación nutricional, las consideraciones bioéticas clave incluyen: a) Consentimiento informado: Los pacientes deben ser informados de manera completa sobre el propósito de la investigación, los riesgos y los beneficios antes de participar en cualquier estudio, b) No maleficencia: Evitar causar daño a los pacientes mediante intervenciones nutricionales innecesarias o inapropiadas, c) Justicia distributiva: Asegurar que todos los pacientes, independientemente de su condición económica o social, tengan acceso equitativo a los beneficios de la investigación, d) Confidencialidad y protección de datos: Con el uso de tecnologías avanzadas, como la IA, la protección de los datos personales de los pacientes es esencial. Los nutricionistas deben ser conscientes de la importancia de la privacidad y de mantener la confidencialidad de la información sensible, e) Transparencia algorítmica: Los sistemas basados en IA que toman decisiones sobre el tratamiento nutricional deben ser transparentes en cuanto a cómo llegan a sus conclusiones y las bases de datos utilizadas.
5.4. Código de Ética del Nutricionista Clínico (FELANPE, 2021) (74).
El Código de Ética del Nutricionista Clínico, promulgado por la FELANPE (Federación Latinoamericana de Nutrición de Terapia Nutricional, nutrición clínica y Metabolismo), es un marco deontológico clave que guía la práctica ética y profesional de los nutricionistas en Latinoamérica y la Península Ibérica. Este código establece los principios fundamentales que los nutricionistas deben seguir, reconociendo los rápidos avances científicos y tecnológicos que generan nuevos dilemas éticos (74).
Principios Deontológicos Adaptados
- Respeto por la dignidad humana: Valorar el contexto cultural y las preferencias individuales, garantizando acceso al cuidado nutricional continuo y personalizado.
- Protección de la persona en condición de vulnerabilidad nutricional: Defensa del derecho humano a la alimentación y a la terapia nutricional, promoviendo la justicia distributiva.
- Respeto por la autonomía: Garantizar que los pacientes tomen decisiones informadas sobre su salud, a través de un consentimiento continuo y asegurando la confidencialidad.
- Adecuación terapéutica: Aplicar la terapia nutricional según principios de beneficencia y no maleficencia, con base en la nutrición basada en evidencia (NUBE) y el juicio clínico interdisciplinario.
- Investigación y desarrollo profesional: Fomentar la formación continua, la transparencia en la investigación y la declaración de conflictos de interés (74).
Implicaciones prácticas: Los algoritmos de IA y las fórmulas innovadoras deben ser evaluados conforme a estos principios, asegurando que la digitalización y la sostenibilidad no comprometan la dignidad ni la igualdad de acceso en la atención nutricional.
5.5. Funciones y Competencias del Nutricionista Clínico (Consenso FELANPE-SENPE, 2023) (75).
El perfil profesional del nutricionista clínico debe estar basado en un modelo profesional armonizado que optimice la aplicación de la nutrición clínica, buscando el beneficio tanto del paciente como del sistema de salud. Este consenso, elaborado por el Comité de Nutricionistas de FELANPE con el apoyo de SENPE, define las competencias y funciones clave de los nutricionistas clínicos (75): Ámbitos de desempeño: Hospitales, unidades de soporte nutricional, atención ambulatoria, programas de APS y domicilios; Competencias asistenciales:
Evaluación, diagnóstico, intervención y monitoreo nutricional; Competencias administrativas: Gestión de calidad, indicadores, compras y producción de fórmulas; Competencias de docencia e investigación: Diseño de protocolos, publicación y difusión de resultados con transparencia.
Impacto esperado: Un perfil profesional estandarizado y bien definido contribuirá a reducir la desnutrición hospitalaria, mejorará los resultados clínicos y facilitará la movilidad profesional dentro de la región.
5.6. Modelo de Proceso de Cuidado Nutricional: consenso para Latinoamérica (76).
El consenso de expertos latinoamericanos propone un modelo didáctico de cinco pasos y cinco pilares para sistematizar el cuidado nutricional, alineado con el Principio 2 de la Declaración Internacional de Cartagena (76).
- Fortalezas: amplia participación de especialistas de distintos países y cobertura integral de las fases del proceso de cuidado nutricional (76).
- Limitaciones: construcción del cuestionario basada en modelos preexistentes, posible sesgo hacia expertos de Colombia y México, y exclusión de algunos indicadores de gestión o herramientas de tamizaje (76).
- Aplicación práctica: herramienta adaptable a las necesidades de cada institución y contexto nacional, orientada a mejorar la calidad, la eficiencia y la enseñanza del cuidado nutricional en todos los niveles de atención (76).
Este modelo complementa los marcos éticos y de competencias previamente descritos, proporcionando una guía operativa para implementar un cuidado nutricional equitativo, transparente y de alta calidad en Latinoamérica.
Mensajes principales: 1-Liderazgo en investigación: El Nutricionista Clínico (NC) conduce estudios desde la formulación hasta la divulgación, combinando rigor metodológico y colaboración multidisciplinaria. 2-Decisiones de MBE/NUBE – medicina basada en evidencia-: Aplica la jerarquía de evidencia y metaanálisis con juicio crítico para diseñar intervenciones precisas. 3-Nutrición de precisión:
Usa datos ómicos (genómica, metabolómica, proteómica) para individualizar dietas.4- Costes y barreras: Valora el impacto económico de la malnutrición (costes ocultos), supera limitaciones de tiempo y recursos. 5-Digitalización e IA: Emplea big data (datos masivos), algoritmos predictivos, imagen y monitorización remota para personalizar y optimizar el cuidado. 6- Ética y equidad: Garantiza transparencia, consentimiento informado, justicia distributiva y corrección de sesgos.
Conclusiones
Esta actualización, ha puesto de manifiesto cómo la investigación es un pilar fundamental en la mejora continua de la nutrición clínica, tanto a nivel práctico como científico. La investigación no solo permite mejorar cada día, sino que también proporciona herramientas para ofrecer a nuestros pacientes un enfoque nutricional más eficaz y exitoso. Además, aumenta el espíritu crítico y profesional, impulsándonos a cuestionar y analizar constantemente la práctica clínica.
En este recorrido, se ha descrito brevemente la historia de la nutrición clínica, destacando cómo los avances científicos han transformado la disciplina. También se han mostrado las dificultades que surgen en el proceso investigativo, con el objetivo de abrir la puerta a una mejor comprensión de los problemas que se enfrentan en la práctica diaria y las soluciones posibles.
Es crucial destacar el papel del nutricionista clínico en la investigación, un rol que muchas veces pasa desapercibidos en los equipos de salud. Es importante motivar a nuestros colegas para que se involucren más activamente en la investigación, reconociendo la trascendencia de la Medicina Basada en Evidencia (MBE) y la Nutrición Basada en Evidencia (NUBE) en la mejora de los resultados clínicos. Además, se deben abordar tanto los beneficios como las críticas planteadas en los metaanálisis, y enfatizar la importancia de tomar en cuenta los costos asociados a las intervenciones nutricionales, las cuales pueden justificar y optimizar la asignación de recursos en el sistema de salud.
Una gran crítica que enfrenta el Nutricionista Clínico es la falta de un resumen crítico y organizado por especialidad o subespecialidad, que incluya de manera periódica todos los estudios aleatorios y controlados relevantes. Este vacío de información dificulta la actualización continua y la toma de decisiones informadas, lo que resalta la necesidad de estructuras de revisión y actualización constante para los nutricionistas clínicos.
En conclusión, la investigación en nutrición clínica no solo permite responder de manera más efectiva a los desafíos del presente, sino que también abre nuevas perspectivas para el futuro. Al integrar la investigación, la MBE/NUBE y las tecnologías emergentes como la inteligencia artificial, el nutricionista clínico no solo se adapta a los avances, sino que se convierte en un líder en la mejora continua de la atención nutricional. Es fundamental que se siga consolidando la dinámica de su participación en la investigación para garantizar que las decisiones clínicas sean cada vez más fundamentadas en la mejor evidencia disponible, siempre centradas en la salud y el bienestar del paciente.
Referencias Bibliográficas
- Jadad AR, Rennie D. The randomized controlled trial gets a middle-aged checkup. JAMA. 1998; 279(4):319-320. doi: 10.1001/jama.279.4.319.
- Jaramillo O. Carta del presidente “Ir en busca…”. Lecturas sobre Nutrición. FELANPE y la Asociación Colombiana de Nutrición Clínica. 1999;(6) 2:1.
- Ladd WS. The function of the hospital dietitian. J Am Diet Assoc. 1925; 1:118-127.
- Peabody FW. The function of the hospital dietitian. J Am Diet Assoc. 1925; 1:82-83.
- Wilder RM. The hospital nutrition expertec. J Am Diet Assoc. 1925; 1:82-83.
- Mac Eachan MT. Advances in dietetics from the hospital viewpoint. J Am Diet Assoc. 1949; 25:494- 496.
- Noland MS, Steinberg R. Activities of therapeutic dietitians-A survey report. J Am Diet Assoc. 1965; 46:477-481.
- Butterworth CE. The skeleton in the hospital closet. Nutr Today. 1974; 9 (2):4-8.
- Tobias AL, Vanitallie TB. Nutritional problems of hospitalized patients. J Am Diet Assoc. 1977; 71:253- 257.
- Bristian BR, Blackburn L, Vitale J et al. Prevalences of malnutrición in general medical patients. JAMA.1976;235:1567-1570.
- Wade J. Role of a clinical dietitian specialist on nutrition support service. J Am Diet Assoc. 1977; 70:185-189.
- A.D.A. Reports. Position paper on clinical dietetics. J Am Diet Assoc. 1982; 80:256-260.
- Forcier JI, Kinght MA, Sheehan ET. Poin of view: Acculturation in clinical dietetics. J Am Diet Assoc. 1977; 70:181-185.
- Butterworth CE. Malnutrition in Hospital. JAMA1974; 230(6):858-879
- Schiller R. Research activities and interests of dietitian. JPEN. 1988;12(1):1-7.
- Smitherman AL, Wyse BW. President’s page: the Black bone of our profession. J Am Diet Assoc. 1987; 87:1394.
- Rose JC. Research or practice. J Am Diet Assoc.1985;85:797.
- Monsen E. Editor´s Outlook. J Am Diet Assoc.1989;89:1591.
- Sims LS, Simko MD. Applying research methods in nutrition and dietetics: Embodiment of the profession´s backbone. J Am Diet Assoc. 1988; 88:1045.
- Dougherty D. President’s page: The strategic plan: the vision. J Am Diet Assoc. 1989; 89:110.
- Wylie-Rosett J, Wheeler M, Krueger M, et al. Opportunities for research-oriented dietitians. J Am Diet Assoc. 1990; 90:1531-4.
- Howard AJ, Ferguson M, Wilkinson P, Campbell KL. Dietetic professional practice. Involvement in research activities and factors influencing research capacity among dietitians. J Hum Nutr Diet. 2013;26(Suppl.1):180-187.
- Kondrup J et al., ESPEN Guidelines for Nutrition Screening 2002. Clin Nut. 2003;22(4):415-421.
- Leistra E. et al. Predictors for achieving protein and energy requirements in undernourished hospital patients. Clin Nutr 2014; 33:495-501. DOI: 10.1016/j.clnu.2011.01.008
- Jager-Wittenaar, H., Sealy, M., Naumann, E., & de van der Schueren, M. Nutritional risk screening: A need to guide Alice in Nutrition and. Current Opinion. Clin Nutr Metab Care. 2024, 27(5), 381-386. https://doi.org/10.1097/MCO.0000000000001051
- Lozano JM. Epidemiología Clínica: Investigación Clínica Aplicada. In: Ruíz, A, Morillo LE. Editorial médica panamericana Ltda Investigación en salud: Qué es y para qué sirve. vol. 1. Bogotá D.F-Colombia: Editorial médica panamericana Ltda.; 2004; p. 19-27.
- Commission on Health Research for Development. Health research: essential link to equity in development. Oxford: Oxford University Press; 1990.
- Henry H. Nutrition education research project example: An experimental design to test the effectives of two nutrition education protocols in reducing serum cholesterol. J Am Diet Assoc.1988;88:1066.
- Drolet, B. C., & Lorenzi, N. M. *Translational research: Understanding the continuum from bench to bedside*. *Translational Research, 2011. 157*(1), 1–5. [https://doi.org/10.1016/j.trsl.2010.10.002] (https://doi.org/10.1016/j.trsl.2010.10.002)
- Monsen ER, Cheney CL. Research methods in nutrition and dietetics, design, data analysis and presentation. J Am Diet Assoc. 1988; 88:1047.
- Ullrich J. Clinical research project example requiring no additional resources: A cohort study on the impact of verbal contact in archiving revision of physician diet prescription. J Am Diet Assoc. 1988; 88:1068.
- Hunter TN. The story of nutrition. In Steffe rad Aied: Food: The yearbook of agriculture for 1959. Washington DC: Us Government Printing office. 1959.
- Dwyer J. Scientific under pinnings for the profession: Dietitians in research. J Am Diet Assoc. 1977; 6:593- 597.
- Why Registered Dietitian Nutritionists Are Not Doing Research-Perceptions, Barriers, and Participation in Research from the Academy’s Dietetics Practice- Based Research Network Needs Assessment Survey. J Acad Nutr Diet. 2015. Enlace: https://www.jandonline.org/article/S2212-2672(15)00118-5/fulltext Revised 2017 Scope of Practice for the Registered Dietitian Nutritionist. J Acad Nutr Diet. 2017. Enlace: https://www.jandonline.org/article/S2212-2672(17)31624-6/pdf
- Carol Ireton-Jone, Stacey B, Gottschich M, Nelson J. Research Nutrition Support Dietetics Core Curriculum. 2nd ed. 1993. p. 497-503.
- Linetzky Waitzberg DL, Torrinhas RM, Correia I. Metodología de la Investigación de Nutrición. Nutrición Enteral y Parenteral. En Arenas MH. Anaya PR. México: Editorial McGraw Hill Interamericana; 2007. p. 576-591.
- Sackett D, Straus S, Richardson WS, Rosenberg W, Haynes RB. Medicina Basada en la Evidencia: Cómo practicar y enseñar la MBE. Edición en español. Madrid-España: Ediciones Harcourt S.A.; 2001. p. 2-9.
- Ruíz Á. Medicina Basada en la Evidencia. Epidemiología Clínica: Investigación Clínica Aplicada. In: Ruíz A, Morillo LE. Ltdavol. 30. Bogotá D.F-Colombia: Editorial médica panamericana Ltda.; 2004; p. 526-537.
- Guyatt G, Sinclair J, Cook D, et al. Grading Recommendations: a Qualitative Approach. In: Guyatt G, Rennie D, eds. User’s Guides to the Medical Literature. Chicago: AMA Press; 2002.
- Sackett DL, Rosenberg WM, Gray JA, Haynes RB, Richardson WS. Evidence based medicine: what it is and what it isn’t. BMJ. 1996; 312:71-2.
- Tajer C. Haciendo posible el debate sobre la medicina basada en evidencias. Rev argen cardiol. 2010;78(5):459-466.
- Lelorier J, Grégoire G, Benhaddad A et al. Discrepancies Between Meta-Analyses and Subsequent Large Randomized, Controlled Trials. N Engl J Med 1997; 337(8):536-542. DOI: 10.1056/NEJM19970821337080.
- Villar J, Carroli G, Belizán JM. Predictive ability of metanalyses of randomised controlled trials. Lancet. 1995; 25;345(8952):772-6.
- Kuhn T. The structure of Scientific Revolutions. México DF: Fondo de Cultura Económica; 1971.
- Serra M L. Nutrición basada en la evidencia (NUBE). Rev Esp Nutr Comun. 2000;6(1)5-6.
- Rodríguez S. Educación médica, aprendizaje basado en problemas. vol. 1. México: Panamericana; 2003. p. 1-10.
- Miján A, De Mateo B. Investigación en nutrición: de la clínica a la mejor evidencia científica. Nutrición Hospitalaria. 2011;26 (2):249-250.
- Meinert CL. Meta-analysis: science or religion? Controlled Clinical Trials. 10(4suppl): 1989;57s-263s.
- Bengoa JM. Evolución de la desnutrición mundial en el siglo XX. An Venez Ntr. 2005;18(2):190-194.
- Tappenden KA et al. JPEN J Parenter Enteral Nutr. 2013; 37:482-497.
- Waitzberg DL Caiaffa WT, Correia MITD. Hospital malnutrition: the Brazilian national survey (IBRANUTRI): a study of 4000 patients. Nutrition. 2001; 17(7-8):573-80.
- Stratton RJ, Green CJ, Ella M. Disease-related malnutrition. CABI Publishing; 2003.
- Stratton R, Elias M. A review of reviews: a new look at the evidence for oral nutritional supplements in clinical practice Clin Nutr 2007; 2:5-23.
- Waitzberg DL, ASPEN ICNSO Symposium Worldwide Differences relater. Implementation of Hospital Nutrition Assessment. Nutrition week Phoenix Az. 2007.
- Abugroun, A., Daoud, H., Hallak, O., Abdel-Rahman, M. E., & Klein, L. W. Frailty predicts adverse outcomes in older patients undergoing transcatheter aortic valve replacement (TAVR): From the National Inpatient Sample. Cardiovasc Revasc Med 2022;34: 56–60. https://doi.org/10.1016/j.carrev.2021.02.004
- Guenter, P., Abdelhadi, R., Anthony, P., Blackmer, A., Malone, A., Mirtallo, J. M., Phillips, W., & Resnick, H. E. (2021). Malnutrition diagnoses and associated outcomes in hospitalized patients: United States, 2018. Nutr Clin Pract 2021;36(5):957-969. https://doi.org/10.1002/ncp.10771
- Correia, M. I. T. D., Castro, M., de Oliveira Toledo, D., Farah, D., Sansone, D., de Morais Andrade, T. R., de Araújo, G. T. B., & Fonseca, M. C. M. Nutrition therapy cost-effectiveness model indicating how nutrition may contribute to the efficiency and financial sustainability of the health systems. JPEN 2021; 45(7), 1542–1550. https://doi.org/10.1002/jpen.2052.
- Zhang, H., Wang, Y., Jiang, Z.-M., Kondrup, J., Fang, H., Andrews, M., Nolan, M. T., Mu, S.-Y., Zhang, J., Yu, K., Lu, Q., & Kang, W.-M. Impact of nutrition support on clinical outcome and cost-effectiveness analysis in patients at nutritional risk: A prospective cohort study with propensity score matching. Nutrition 2017;37, 53–59. https://doi.org/10.1016/j.nut.2016.12.004.
- The American Medicine Institute in its Health Care Quality Committee its Health Care Quality Committee List for the XXI century and its application in the List for the XXI century and its application in the Nutritional Support Area Nutritional Support Area Institute of Medicine (US) Committee on Quality of Health Care in America. Washington (DC): National Academies Press (US); 2001.
- Montoya et al. Efecto de la intervención nutricional temprana en el resultado clínico de pacientes en riesgo nutricional. Nutr Hosp. 2014;29(2):427-436.
- Oliveira G. Costs versus benefits of oral nutritional supplements. Nutr Hosp. 2009;24(3):251-259.
- Gómez Candela C. Efficacy, cost-effectiveness, and effects on quality of life of nutritional supplementation Nutr Hosp. 2010;25(5):781-92.
- Winkler M. Improving Safety and Reducing Harm Associated with Specialized Nutrition Support. Nutr Clin Pract. 2005;20(6):595-596.
- Jencks SF, Williams MV, Coleman EA. Re hospitalización de pacientes de los servicios del programa de medicare. N Engl J Med. 2009; 360:1418- 1428.
- Gomes, F., Baumgartner, A., Bounoure, L., et al. Association of nutritional support with clinical outcomes among medical inpatients who are malnourished or at nutritional risk: An updated systematic review and meta-analysis. JAMA 2019;2(11), e1915138. https://doi.org/10.1001/jamanetworkopen.2019.15138
- Kaegi-Braun, N., Germann, S., Faessli, M., et al. Effect of micronutrient supplementation in addition to nutritional therapy on clinical outcomes of medical inpatients: Results of an updated systematic review and meta-analysis. Eur J Clin Nutr 2022; 76(7), 964–972. https://doi.org/10.1038/s41430-021-01061-7
- Zhong, J. X., Kang, K., & Shu, X. L. Effect of nutritional support on clinical outcomes in perioperative malnourished patients: A meta-analysis. Asia Pac J Clin Nutr 2015; 24(3), 367–378. https://doi.org/10.6133/apjcn.2015.24.3.20
- Pérez JIU, Picón CMJ, Benvent EG, Alvarez EM. Detección precoz y control de la desnutrición hospitalaria. J Nutr Hosp. 2002;17(3):139-46.
- Matusheski, N. V., Caffrey, A., Christensen, L., et al. Diets, nutrients, genes and the microbiome: Recent advances in personalised nutrition. British J Nutr. 2021; 126(10), 1489-1497. https://doi.org/10.1017/S0007114521000374
- Voruganti, V. S. Precision nutrition: Recent advances in obesity. Physiology 2023, 38(1): 42-50. https://doi.org/10.1152/physiol.00014.2022
- de Toro-Martín, J., Arsenault, B. J., Després, J. P., & Vohl, M. C. Precision nutrition: A review of personalized nutritional approaches for the prevention and management of metabolic syndrome. Nutrients 2017; 9(8), 913. https://doi.org/10.3390/nu9080913
- Matusheski, N. V., Caffrey, A., Christensen, L., et al. (2021). Diets, nutrients, genes and the microbiome: Recent advances in personalised nutrition. British J Nutr 2021; 126(10), 1489–1497. https://doi.org/10.1017/S0007114521000374
- Parchure, P., Besculides, M., Zhan, S., Cheng, F.-Y., Timsina, P, Cheertirala, S. N., Kersch, I., Wilson, S., Freeman, R., & Reich, D. Malnutrition risk assessment using a machine learning-based screening tool: A multicentre retrospective cohort. J Hum Nutr Diet 2024; 37(3): 622-632. https://doi.org/10.1111/jhn.13286-
- Sierra Tobón, L. M., López Talavera, M., Pérez Cano, A., Maza Moscoso, C., Senese, A., Van Aanholt, D., Rodríguez, J. K., Sepúlveda, C. et al. FELANPE’s Code of Ethics for the Clinical Nutritionists [Código de ética do nutricionista clínico do FELANPE]. Rev Nutr Clin Metab 2021; 4(Supl. 1):110-113. https://doi.org/10.35454/rncm.v4supl1.350
- Canicoba, M., de Baptista, G. A., & Visconti, G. Funciones y competencias del nutricionista clínico: Documento de consenso. Una revisión de diferentes posiciones de sociedades científicas latinoamericanas. Rev Cubana Aliment Nutr 2013; 23(1), 146-172.
- Pérez Cano, A. M., Díaz, G., Maza Moscoso, C. P., Castro Muñoz, M. G., Canicoba, M., González, M. C., Barbosa, J., Calvo, I., Adrianza de Baptista, G, et al. Modelo de proceso de cuidado nutricional: consenso para Latinoamérica. Rev Nutr Clin Metab 2022; 5(4): 38-50. https://doi.org/10.35454/rncm.v5n4.433.
