La educación nutricional es una herramienta que promueve la creación de hábitos alimentarios. Los suplementos dietéticos se definen como productos elaborados con nutrientes y otros componentes presentes en los alimentos con el propósito de satisfacer las necesidades nutricionales en términos de cantidad o calidad, para mantener o mejorar el estado nutricional. La intervención nutricional apoyada en la práctica de la lactancia materna, una alimentación equilibrada, variada y con alimentos localmente disponibles, junto con el manejo adecuado de hábitos y conductas de alimentación e intervenciones en agua, saneamiento, higiene y salud; deben siempre acompañar al uso de suplementos dietéticos. Los suplementos dietéticos, especialmente los que contienen vitaminas y minerales, pueden ser empleados con fines preventivos o curativos. Existen recomendaciones preventivas en la edad pediátrica para hierro, zinc, fluor, yodo y vitaminas A y D; incluyendo el uso de micronutrientes en polvo, una estrategia para fortificar los alimentos en el hogar. El personal de salud debe manejar adecuadamente las recomendaciones preventivas de los SD de vitaminas y minerales, especialmente en la atención de los grupos más vulnerables: embarazadas, madres lactantes y niños menores de 5 años de edad. An Venez Nutr 2020; 33(2): 169-176.
Palabras clave: Nutrición del niño, suplementos dietéticos, medicamentos a base de vitaminas y minerales, anemia ferropénica, deficiencia de hierro, deficiencia de vitamina A, micronutrientes.
Dietary supplements are defined as products made with nutrients and other components present in foods in order to meet nutritional needs in terms of quantity or quality, to maintain or improve nutritional status. Nutritional intervention supported by the practice of breastfeeding, a balanced, varied diet with locally available foods, along with proper eating habits and behaviors and interventions in water, sanitation, hygiene and health; should always accompany the use of dietary supplements. Dietary supplements, especially those containing vitamins and minerals, can be used for preventive or curative purposes. There are preventive recommendations in the pediatric age for iron, zinc, fluoride, iodine and vitamins A and D; including the use of micronutrients powder, a strategy to fortify food at home. Health workers should adequately manage preventive recommendations for vitamin and mineral dietary supplements, especially in the care of the most vulnerable groups: pregnant women, nursing mothers and children under 5 years of age. An Venez Nutr 2020; 33(2):169-176.
Key words: Child nutrition, dietary supplements, drugs on basis of vitamins and minerals, iron-deficiency anemia, iron deficiency, vitamin A deficiency, micronutrients.
Correspondencia: Mariana Mariño Elizondo, mmarino.cania@gmail.com
Los suplementos dietéticos (SD) o complementos alimenticos (CA) se definen como productos elaborados a base de nutrientes y otros componentes presentes en los alimentos, llamados “ingredientes dietéticos”, con el propósito de incrementar la ingesta dietética total, complementarla o suplir algún componente; para así contribuir a mantener o mejorar el estado nutricional. Los ingredientes dietéticos incluyen vitaminas hidro y liposolubles, ácidos grasos esenciales, minerales, aminoácidos, hierbas o productos botánicos (1).
En la legislación venezolana se encuentra la siguiente definición, Suplemento dietario: “Es aquel producto cuyo propósito es adicionar la dieta normal y que es fuente concentrada de Nutrientes y otras sustancias con efecto fisiológico o nutricional que puede contener vitaminas, minerales, proteínas, aminoácidos, otros nutrientes y derivados de nutrientes, plantas, concentrados y extractos de plantas solas o en combinación” (2).
Los SD se encuentran en diversas presentaciones: tabletas, cápsulas, líquidos, polvo y barras (1) que contienen un solo componente o combinación de ellos, como es el caso de los multivitamínicos con minerales. Estos productos son considerados alimentos y no medicamentos, por lo tanto, no están sujetos a estudios de seguridad y eficacia. Sin embargo, muchos SD pueden contener ingredientes con efectos biológicos, incluso hay productos que contienen medicamentos ocultos que se comercializan a veces falsamente como suplementos dietéticos (3). Por tanto, se debe insistir en que la población consulte con un profesional de la salud antes de iniciar el consumo de cualquier SD.
En América Latina la denominación de estos productos no está estandarizada u homologada, observándose en los instrumentos legales, designaciones de complementos alimenticios o suplementos dietéticos, dietarios, alimenticios o nutricionales (4).
En la mayoría de los países los SD al ser considerados alimentos su regulación se rige por los instrumentos legales propios de esta materia. Panamá es una excepción, ya que en el año 2019 aprobó las normas para el proceso de inscripción sanitaria de Suplementos Vitamínicos, Dietéticos y Alimenticios con Propiedades Terapéuticas, considerando que un suplemento dietético deja de ser tal y adquiere la categoría de medicamento cuando en su rotulación se establece que está destinado a prevenir, tratar o curar cualquier enfermedad.
Incluye en esta categoría todos los productos cuyas concentraciones en su formulación sobrepasen los requerimientos nutricionales establecidos por la Organización Mundial de la Salud (OMS) y se indiquen para una condición clínica específica (5).
En el mercado venezolano no existe uniformidad en la denominación de productos con vitaminas u otros ingredientes dietéticos esenciales para la nutrición, y pueden ser comercializados bajo el nombre de complemento alimenticio o suplemento dietético, aunque tengan la misma composición. Esta situación puede tener explicación, ya que al ser considerados alimentos deben regirse por los diferentes instrumentos legales que regulan la materia, los cuales no están armonizados ni actualizados (4).
Para efectos de la expedición del Registro Sanitario de alimentos que autoriza su comercialización, el órgano competente es el Ministerio del Poder Popular para la Salud, a través del Servicio Autónomo de Contraloría Sanitaria (4).
Los diferentes instrumentos del marco regulatorio de los complementos alimenticios en el país son:
A nivel mundial existe interés en el desarrollo de un marco normativo armonizado sobre complementos alimenticios, en el cual se ha avanzado mucho durante estas dos últimas décadas (11).
La práctica de la lactancia materna exclusiva hasta los 6 meses, seguida de la incorporación de la alimentación complementaria óptima que garantice el consumo de una amplia variedad de alimentos naturales en cantidades adecuadas, es la mejor manera de mantener la salud y prevenir enfermedades crónicas (12,13), sin embargo, considerando la prevalencia de alteraciones nutricionales poblacionales e individuales, condiciones fisiológicas, ciclo de vida, presencia de patologías y dietas especiales; se han establecido recomendaciones particulares para el uso de SD (14-21).
Idealmente toda intervención de suplementación de nutrientes debe ir acompañada de estrategias destinadas a reducir la inseguridad alimentaria, aumentar la diversidad de la dieta, promoción de lactancia materna y buenas prácticas de higiene y alimentación.
Reportes recientes señalan que el 34% de los niños y adolescentes en Estados Unidos consume suplementos nutricionales, en su mayoría multivitamínicos combinado con minerales (22,23). En la minoría de los casos, 15 a 18%, el uso de SD es por indicación médica, los motivos más frecuentes para su consumo son mejorar o mantener el estado de salud o como complemento de la dieta (24,25).
Se ha establecido que durante la gestación los nutrientes en riesgo de déficit incluyen; ácido fólico, vitamina D, iodo, hierro magnesio, colina, carotenoides y ácidos grasos omega-3 (26). Por otro lado, durante el embarazo la suplementación de vitamina A y E, en regiones con alta prevalencia de deficiencia, ha mostrado beneficios para la salud materna. La suplementación de hierro y ácido fólico ha sido extensamente estudiada y constituye una clara recomendación. También se ha demostrado beneficios del uso de ácidos grasos omega-3 y colina. En el caso del zinc se considera necesario ampliar las investigaciones (26).
En los niños entre los 0 y 24 meses, aunque la ingesta es variable, los datos sugieren un bajo consumo de: vitamina D, colina, ácidos grasos omega-3, iodo y hierro (26). Por otra parte, la leche humana ha sido señalada en algunos estudios, como deficiente en hierro, iodo, ácido fólico y vitamina D; por tanto, la suplementación de la madre o de su hijo con estos nutrientes durante la lactancia exclusiva, ha sido recomendada (26). La Academia Americana de Pediatra (AAP) recomienda el consumo de multivitamínicos durante la gestación y lactancia (27) y en los menores de dos años de edad hierro y vitamina D, de igual manera, la OMS y otras agencias internacionales han establecido recomendaciones para estos y otros nutrientes (15,28-32).
Hierro: con el objetivo de prevenir la deficiencia de hierro y anemia la OMS recomienda la suplementación de este mineral en poblaciones donde la prevalencia de anemia sea igual o mayor al 40%. En regiones donde se desconoce esta cifra, debe asumirse una condición de alta prevalencia (28,32).
Aunque en el país no se cuenta con cifras oficiales de la prevalencia de déficit de hierro y anemia, diversos estudios han reportado cifras superiores al 40% en distintos grupos poblacionales (33).
La suplementación propuesta es una estrategia preventiva poblacional, que sugiere tratamiento consecutivo durante 3 meses en un año, para niños de 6 - 23 meses de edad, 24 -59 meses y 5 - 12 años con 10 - 12,5 mg de hierro elemental/día, 30 mg de hierro elemental/día y 30 - 60 mg de hierro elemental/día respectivamente (28).
En poblaciones preescolares y escolares con prevalencia de anemia entre 20% y 40% se recomienda la suplementación intermitente, administrando hierro un día por semana durante tres meses; seguido de 3 meses sin suplementación durante todo el calendario escolar. La dosis recomendada es de 25 mg de hierro elemental para niños entre 24 - 59 meses y 45 mg de hierro elemental para niños y adolescentes entre 5 - 12 años (32).
En el grupo de adolescentes postmenarquia no embarazadas de áreas con prevalencia de anemia igual o mayor a 20% se recomienda la suplementación intermitente de 60 mg de hierro elemental más 2,8 mg de ácido fólico, administrado un día por semana durante 3 meses, seguido de 3 meses sin suplementación, en este mismo grupo si la prevalencia de anemia es superior a 40% la dosis de hierro elemental asciende a 30- 60 mg/día por 3 meses consecutivos (18-20,28).
En poblaciones donde la prevalencia de parasitosis intestinal es de 20% o más el tratamiento antiparasitario universal al menos una vez al año para mayores de 5 años de edad, combinado con la suplementación de hierro debe ser considerado (32).
Vitamina D: durante los primeros meses de vida, los niveles de vitamina D dependen de los depósitos del recién nacido, el aporte de la alimentación, la exposición solar o los suplementos de vitaminas. Como el contenido de vitamina D de la leche humana depende de las reservas maternas de vitamina D, que a menudo son escasas y si la exposición al sol no es posible, los niños amamantados estarán en riesgo de presentar déficit de vitamina D. Aunque se han llevado a cabo revisiones sistemáticas, no se dispone aún de directrices aprobadas por el Comité de Examen de Directrices de la OMS (34); sin embargo, diversas sociedades pediátricas internacionales consideran razonable recomendar un suplemento diario de 400 UI de vitamina D, durante el primer año de vida, a partir del egreso del hospital o de los 15 días, tanto si el niño recibe leche materna como si se alimenta con fórmulas lácteas infantiles con una ingesta menor de un litro de leche al día. En los niños prematuros menores de 1 año de edad corregida, la dosis de vitamina D debe ser de 200 – 400 UI/día (15,29-31). La revisión más reciente de los valores de referencia de energía para la población venezolana, recomienda 400 UI de vitamina D para menores de 2 años de edad (35). En el mercado nacional hasta el momento no se cuenta con formulaciones pediátricas solo con vitamina D, la misma se presenta combinada con otros micronutrientes; especialmente con vitamina A y C.
Vitamina A: en los entornos en que la carencia de vitamina A constituye un problema de salud pública, se recomienda administrar suplementos de vitamina A a lactantes y niños de 6 a 59 meses de edad como intervención de salud pública para reducir su morbimortalidad (36). En las poblaciones con una prevalencia de ceguera nocturna igual o mayor a 1% en niños de 24 a 59 meses o con una prevalencia de carencia de vitamina A (contracción sérica de retinol igual o menor a 0,70 μmol/l) igual o mayor a 20%, los lactantes y niños de 6 a 59 meses, deben ser suplementados (36). En Venezuela, la deficiencia de vitamina A medida por retinol sérico, varía en diferentes grupos de edad entre 14-26% (37).
La dosis recomendada es de 100000 UI vía oral en dosis única para niños entre 6 -11 meses y de 200000 UI cada 4 a 6 meses en niños entre 12-59 meses (32,36). En los niños con dietas de bajo aporte de vitamina A, la suplementación con una dosis alta de vitamina A, solo mejora el estado nutricional por tres meses; por esta razón, esta intervención debe acompañarse de acciones complementarias como biofortificación, micronutrientes en polvo, diversificación de la dieta, educación nutricional y prevención y control de infecciones (38).
Zinc: los niños nacidos de madres con déficit nutricional que después del nacimiento consumen dietas con bajo contenido de zinc y viven en condiciones sanitarias deficientes con la consecuente inflamación intestinal y sistémica, son una población con riesgo de déficit de zinc, sin embargo, la suplementación solo está indicada en casos de diarrea en cualquier tipo de contexto, con el fin de reducir la severidad, la mortalidad y subsecuentes episodios de la enfermedad. Se recomienda administrar 20 mg/día de sulfato zinc durante 10–14 días, a todos los niños con diarrea. Para niños menores de 6 meses de edad, la dosis del zinc debe ser de 10 mg/día (15,39,40). En cuanto a suplementación de zinc y crecimiento la OMS recomienda continuar las investigaciones para poder hacer recomendaciones específicas (41). En Venezuela no se cuenta con presentaciones comerciales de este suplemento, debiéndose indicar preparaciones de formulaciones farmacéuticas de sulfato de zinc al 5% que tienen las limitantes de su sabor, efectos gastrointestinales y necesidad de refrigeración.
Yodo: la recomendación de suplementación está basada en el porcentaje de hogares con acceso a sal yodada. En Venezuela desde el año 2002, se ha venido reportando un deterioro en la calidad de la sal que se consume en las comunidades de mayor riesgo para los trastornos por deficiencia de yodo, ya que desde entonces no se logra alcanzar el nivel recomendado de 90% con contenido adecuado de yodo para muestras en hogares (33,42). De igual manera, se ha encontrado un incumplimiento constante de la norma nacional de yodación de sal (40-70 mg/kg de sal), que viene descendiendo de 43,5% a 34% entre 2001 y 2002 (43).
En embarazadas y mujeres en período de lactancia de países en los que menos del 20% de los hogares tenga acceso a la sal yodada, debe indicarse suplementos de yodo. En países con acceso a sal yodada entre 20% y 90%, debe aumentarse el consumo de yodo con suplementos o alimentos en los grupos más vulnerables (44). La dosis de suplementación recomendada para niños entre 6 y 23 meses de edad es 90 μg/d de yoduro de potasio o 200 mg/año con aceite iodado, para menores de 6 meses la suplementación se hace a través de la leche materna, por lo que la madre debe recibir 250 μg/d (32,44). Los pescados con menor contenido de grasa y las algas marinas, como wakame, nori o mekabu contienen altas cantidades de yodo, la pérdida de nutriente al cocinar del pescado es menor al freír o asar (20%) que al hervir (50%) (45).
Fluor: la suplementación con este mineral es efectiva para reducir la prevalencia de caries dentales, no está recomendada durante los primeros 6 meses; debe ser considerada en niños entre 6 meses y 3 años con alto riesgo de caries, residentes de comunidades donde la fluoración del agua es inferior a 0,3 ppm y en niños y adolescentes entre 6 y 16 años donde la fluoración del agua es inferior a 0,6 ppm (46,47).
Establecer el aporte dietético y de otras fuentes de fluor antes de prescribir su suplementación, puede ayudar a reducir la ingesta excesiva de fluor, que durante periodos críticos del desarrollo dental pueden conducir a fluorosis del esmalte de la dentición definitiva. Las fuentes dietéticas de fluor incluyen el agua para consumo, bebidas como sodas, jugos, fórmulas lácteas infantiles, alimentos preparados y pasta dental (46,47).
Otra recomendación que puede ayudar a reducir la ingesta excesiva de fluor es usar una cantidad de pasta dental fluorada del tamaño de un grano de arroz para niños menores de tres años y del tamaño de un guisante para niños de tres a seis años, así como, enjuagar con agua adecuadamente después de cepillarse para eliminar por completo la pasta dental (46).
Calcio: A pesar de que varios estudios han demostrado que el consumo de calcio está por debajo de los requerimientos nutricionales, especialmente en adolescentes; excepto para las adolescentes embarazadas (18,32) y recién nacidos pre término o de bajo peso al nacer (21), no hay a la fecha recomendaciones específicas para la suplementación con calcio.
La suplementación con micronutrientes en polvo es una estrategia preventiva que permite la fortificación de alimentos en el hogar y está indicada en niños de 6 - 23 meses y de 2 - 12 años, de áreas con prevalencia de anemia igual o mayor al 20% en niños menores de 2 años o menores de 5 años de edad.
Este SD se presenta en sobres de 1 gramo que contienen: hierro: 12,5 mg (fumarato ferroso), sulfato de zinc 5 mg, vitamina A: 999 UI, ácido fólico: 160 ug y vitamina C: 30 mg (48). Su presentación ofrece ventajas operativas de transporte y almacenamiento y menor frecuencia y severidad de efectos secundarios (32).
El esquema recomendado es de un sobre diario agregado al alimento por 90 días, seguido de 90 días de descanso para luego repetir el esquema (48,49).
Con la implementación del Programa de Respuesta Humanitaria en Venezuela, con la participación del Cluster de Nutrición, el uso de los micronutrientes en polvo se ha extendido en la población menor de 5 años (50).
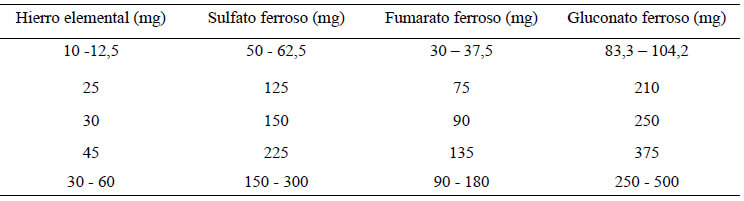
En la selección y dosificación de los SD de vitaminas y minerales es importante conocer la estructura química y la cantidad del mineral elemental contenida en la sal a utilizar. En el Cuadro1 se muestra la equivalencia entre hierro elemental y las sales de uso más frecuente. El carbonato de calcio es la sal con mayor concentración de calcio elemental, requiere de un medio ácido para su óptima absorción, por lo que es recomendable consumirlo con los alimentos, a diferencia del citrato de calcio que puede tomarse con o sin los alimentos. El lactato y gluconato de calcio son de menor utilidad por su bajo contendido de calcio elemental. En cuanto a la absorción del calcio, esta es máxima con dosis de 500 mg (17).
Con relación a la vitamina D, no hay claridad sobre la diferencia en los efectos de la vitamina D2 versus la D3 en el estado nutricional de la vitamina D. Estudios observacionales han señalado que la vitamina D2 (Ergocalciferol) es menos efectiva que la vitamina D3 (Colecalciferol) para mantener valores adecuados de vitamina D, por otra parte, un estudio aleatorio doble ciego en adultos, demostró que , la vitamina D2 es igual de eficaz que la vitamina D3 en el mantenimiento del estado 25-hidroxivitamina D (51) y más recientemente un metanálisis indicó que la vitamina D3 es más eficaz en elevar los niveles de 25(OH)D y potencialmente podría convertirse en la elección para la suplementación (52). El calcifediol (25OHD3) un análogo de la vitamina D ha demostrado ser una alternativa comparable con la vitamina D3 en la prevención y tratamiento de la deficiencia de vitamina D en adultos de distintas edades (53).
Los suplementos dietéticos son productos de amplio uso en nutrición pediátrica, con aplicaciones tanto curativas como preventivas. Los SD no pueden sustituir una alimentación adecuada y su indicación debe siempre ir acompañada de apoyo y promoción de la lactancia materna, educación nutricional, recomendaciones sobre higiene personal, ambiental y pautas sobre estilos de vida saludable. El personal de salud debe manejar adecuadamente las recomendaciones preventivas de los SD de vitaminas y minerales, especialmente en la atención de los grupos más vulnerables: embarazadas, madres lactantes y niños menores de 5 años de edad.
Recibido: 10-01-2021
Aceptado: 30-01-2021